Нелетучесть
Cтраница 2
Общий признак всех полимеров - их нелетучесть; они не перегоняются. При нагревании одни полимеры плавятся без разложения, другие же разлагаются. Вместе с тем плавление полимера имеет свои особенности: они плавятся не при постоянной температуре, а в некоторых границах. [16]
Высокому молекулярному весу углерода соответствует его нелетучесть. С - Л З с С5Н ] 0, то увидим, что в силу замены S на С молекула становится летучее и менее связанной. Хотя из летучих соединений углерода можно получить обычный уголь ( С), но это не требует признания наличия С в любом соединении, так же, как не требуется признания парациана в цианистых соединениях, хотя последние и выделяют его при нагревании. [17]
Именно этим объяснял он тугоплавкость и нелетучесть двуокиси кремния. [18]
Пластификаторы - органические продукты, отличающиеся нелетучестью или весьма незначительной испаряемостью, придающие лакокрасочным пленкам ( покрытиям) необходимую эластичность. [19]
Соединения сполна замещенных аммониев отличаются вообще нелетучестью: при нагревании, йодистый тетрэфиламмоний дает, например, триэфиламин и йодистый эфил, а гидрат этого аммония распадается на триэфиламин, эфилен и воду. [20]
Сходство это, конечно, зависит от нелетучести как бора, так и углерода. [21]
 |
Треугольные диаграммы фазового равновесия. [22] |
При абсолютной нерастворимости ГН в абсорбенте и нелетучести абсорбента А их смесь ( любая точка на линии ГН-А) разделяется на чистый газ-носитель ГН и чистый абсорбент А. Здесь точка Е соответствует максимальной растворимости ПК в абсорбенте А в реальных условиях. При увеличении растворимости ( в результате повышения давления, понижения температуры) точка Е смещается в сторону ПК. [23]
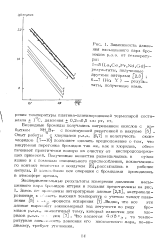 |
Зависимость давления насыщенного пара бромидов р.з.э. от температуры. [24] |
Опыт работы с хлоридами р.з.э. [6,7] и нелетучесть окси-хлоридов [ 7 - 10J позволяет сделать предположение о том, что вакуумная перегонка бромидов так же, как и хлоридов, обеспечивает практически полную их очистку от кислородсодержащих примесей. [25]
Теплоту испарения углерода в одноатомный пар из-за крайней нелетучести углерода не удалось определить на опыте, но для подтверждения гипотезы Менделеева мы можем воспользоваться тем, что из термохимии алифатических соединений известна теплота образования связи С-С, равная 71 ккал ( на авогадрово число N6 02 - Ю23 таких связей), а из кристаллохимии - строение алмаза. [26]
Стационарная жидкая фаза должна удовлетворять следующим требованиям: нелетучесть, химическая инертность, небольшая вязкость, способность образовать равномерную пленку, прочно связанную с носителем. Разделительная способность стационарной фазы для компонентов данной пробы должна быть максимальной. Время удерживания растворенного вещества прямо зависит от коэффициента распределения, который, в свою очередь, определяется свойствами стационарной жидкой фазы. Коэффициент распределения не должен быть ни слишком высоким, ни слишком низким, так как если значение его велико, то время удаления вещества из колонки увеличивается, при низких значениях коэффициента распределения вещество проходит через колонку слишком быстро и разделения не происходит. [27]
Этим объясняются высокие температуры плавления силикатов и их нелетучесть. Это же приводит к свойственной некоторым силикатам способности легко обменивать ионы одних металлов на ионы других. Так, некоторые природные цеолиты или искусственно приготовляемые силикаты при взаимодействии с водными растворами солей могут частично обменивать содержащиеся в них катионы на катионы, имеющиеся в растворе. При этом обязательным условием является, чтобы размеры этих ионов не различались значительно. Так, ионы натрия Na ( радиус 1 05 А) легко обмениваются на ионы кальция Са2 ( радиус 0 95 А) в соотношении 2: 1, причем сохраняется нейтральность кристалла в целом. Искусственные цеолиты используются также в качестве адсорбентов ( молекулярные сита, см. стр. [28]
Этим объясняются высокие температуры плавления силикатов и их нелетучесть. Это же приводит к свойственной некоторым силикатам способности легко обменивать ионы одних металлов на ионы других. Так, некоторые природные цеолиты или искусственно приготовляемые силикаты при взаимодействии с водными растворами солей могут частично обменивать содержащиеся в них катионы на катионы, имеющиеся в растворе. При этом обязательным условием является, чтобы размеры этих ионов не различались значительно. Так, ионы натрия Na ( радиус 1 05 А) легко обмениваются на ионы кальция Са2 ( радиус 0 95 А) в соотношении 2: 1, причем сохраняется нейтральность кристалла в целом. [29]
Обнаружена нестабильность фталоцианинов р.з.э. в кислых средах и нелетучесть при нагревании в вакууме. [30]
Страницы: 1 2 3 4