Ненасыщенность - связь
Cтраница 1
Ненасыщенность связей у поверхностных атомов таких кристаллов часто приводит к изменению симметрии расположения поверхностных атомов в сравнении с объемными, получившему название поверхностной реконструкции. Образование адгезионных связей требует перестройки атомной структуры поверхности и в ряде случаев дополнительной энергии активации. [1]
Ненасыщенностью связей в тетрахлориде циркония объясняется также и образование большого числа координационных соединений как с неорганическими, так и с органическими веществами, в состав которых входят атомы, могущие быть донорами электронов, в первую очередь атомы кислорода и в меньшей степени атомы азота. [2]
Ненасыщенностью связей в тетрахлоридах объясняется также и образование большого числа координационных соединений как с неорганическими, так и органическими лигандами. [3]
Наиболее характерной особенностью атомов поверхностей твердого тела является ненасыщенность связей. Именно поэтому поверхность никеля катализирует, например, реакцию гидрирования ненасы - ценных соединений углерода. На поверхности никеля происходит адсорбция молекул водорода, сопровождающаяся одновременной диссоциацией. [4]
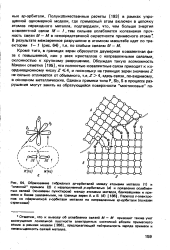
Одна из причин, стимулирующих ионный обмен, - ненасыщенность связей, главным образом, в боковых ответвлениях цепей или лент в структурах дисперсных кристалликов глин. Вторая причина - изоморфные замещения в тетраэдрических ( Si4 на АР) и октаэдрических ( А13 на Mg2) позициях. Это приводит к образованию суммарного отрицательного заряда пакета, который компенсируется адсорбцией катионов. В монтмориллоните и вермикулите ( структуры с межпакетной водой) 80 % адсорбированных ионов размещается между пакетами, а 20 % - на поверхности кристаллов. В противоположность этому в каолините и галлуазите ионы адсорбируются в основном поверхностью кристалла. [5]
Тейлор предложил гипотезу активных центров, согласно которой степень ненасыщенности связей атома в поверхностном слое зависит от его положения в кристаллической решетке. Из этого следует, что поверхностная энергия твердого тела может меняться от точки к точке. Однако такое объяснение сложной структуры поверхности катализатора и специфичности его каталитического действия далеко от истины. [6]
Свободные валентности могут существовать на поверхности твердого тела в результате ненасыщенности связей, но могут и появиться на поверхности кристалла. Всякий ионный кристалл содержит на поверхности и в объеме некоторое количество свободных электронов и свободных дырок. Эти электроны или дырки могут странствовать по кристаллу. Свободный электрон может рассматриваться как положительная валентность, дырка - как свободная отрицательная валентность. [7]
 |
Изменение плотности сво - ( юдной энергии в поверхности разрыва. [8] |
Наличие свободной поверхностной энергии можно объяснить специфической неском-пенсированностью молекулярных сил ( ненасыщенностью связей) на поверхности раздела фаз, вследствие чего образование новой поверхности требует затраты работы на выведение некоторого числа молекул из объема фаз на их поверхность, где взаимодействия между молекулами отличаются от взаимодействий в объеме фаз. Вблизи межфазной поверхности на расстояниях, соизмеримых с размером молекул, характерная для каждой фазы однородность состава и свойств не может сохраняться. Между фазами существует более или менее сильно развитый неоднородный слой, в котором осуществляется переход от свойств, характерных для одной фазы, к свойствам, характерным для другой. [9]
Подвижность липидных молекул и молекул-переносчиков в мембране зависит от температуры и степени ненасыщенности связей между углеродными атомами углеводородных хвостов липидных молекул. [10]
Отметим, что к выводу об ослаблений связей М - М приводит также учет возмущения локальной плотности электронных состояний вблизи примесного атома в рамках модели [286], предполагающей нейтральность заряда примеси и ненасыщенность связей металла. [12]
 |
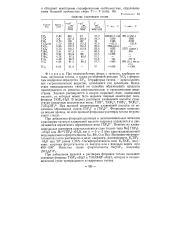
Свойства галогенидов титана. [13] |
Тетрафторид титана - кристаллическое гигроскопическое вещество, плавящееся под давлением. Вследствие ненасыщенности связей он способен образовывать продукты присоединения со многими неорганическими и органическими веществами. Фторидные комплексы весьма прочны, по этой причине фторидные растворы титана не разъедают стекло. [14]
 |
Свойства галогенидов титана. [15] |
Страницы: 1 2