Неоднородность - поверхность - металл
Cтраница 1
Неоднородность поверхности металла на границе раздела металл - электролит приводит к образованию на отдельных участках этого металла различных по величине потенциалов, что вызывает образование коррозионных элементов, электрический ток которых обусловливает электрохимическое растворение металла. [1]
Неоднородность поверхности металла может иметь различный характер. [2]
Вследствие неоднородности поверхности металла, особенно металлических сплавов, например стали, отдельные участки поверхности металла начинают работать как микроэлементы, - таким образом неоднородность металла оказывает прямое влияние на процессы его коррозии ( см. стр. [3]
 |
Сопло пескоструйной камеры. [4] |
Вследствие неоднородности поверхности металла травление вызывает неравномерное изменение шероховатости. Резкое возрастание шероховатости не позволяет рекомендовать травление в качестве предварительной обработки углеродистых сталей. Для легированной стали такое резкое возрастание шероховатости поверхности наблюдается лишь при травлении смесью серной и соляной кислот. [5]
Исходя из неоднородности поверхности металла, мы показали, что при наложении достаточно отрицательного потенциала или при интенсивном перемешивании среды необратимая адсорбция имеет место лишь на части защищаемой поверхности, а на остальной поверхности металла происходит десорбция относительно слабо связанных с твердой поверхностью молекул ПАВ. [6]
Исходя из неоднородности поверхности металла и наличия на них активных в адсорбционном отношении участков с высокой удельной поверхностной энергией ( места с различной кристаллографической ориентацией отдельных кристаллитов, дефекты кристаллической решетки, границы зерен, выступы и углы, трещины, разрывы или слабые места в окисной пленке), отечественными и зарубежными исследователями показано, что не вся доступная поверхность равнозначным образом участвует в образовании прочной связи с адсорбирующимися на ней молекулами. После насыщения ингибитором более активных участков начинается его адсорбция на менее активных участках, что ведет к образованию на металле сплошных пленок с высокой экранирующей способностью. Оба эти процесса идут одновременно: хемосорбция происходит на активных участках, а оставшаяся часть поверхности покрывается ингибитором за счет слабых физических сил. Полагают, что хемосорбционная связь ингибитора с защищаемой поверхностью обусловлена л-электронным взаимодействием свободной пары электронов, имеющихся у атомов азота, фосфора, серы и кислорода с незаполненными электронами cf - оболочки атомов металла. При этом возможно образование координационных ( кова-лентных) связей молекул ингибитора с поверхностными атомами металла, поэтому ингибитор действует как донор электронов, а металл - как их акцептор. [7]
Однако и неоднородность поверхности металла не обязательно приводит к коррозии. Для протекания электролитического процесса необходим анод ( где освобождаются электроны), имеющий электрический контакт с катодом ( на котором электроны потребляются, принимая участие в образовании новых химических соединений), а также электролит, например в виде пленки атмосферной влаги или другой жидкой фазы, в которой ионы могут перемещаться, осуществляя тем самым перенос электрического тока. [8]
 |
Схема электрохимического растворения металла. [9] |
В результате этой неоднородности поверхности металла одни участки в нем играют роль анодов, а другие - катодов. Обычно анодными ( отрицательно заряженными) участками, подверженными растворению, являются менее благородные металлы; катодными ( положительно заряженными) участками, на которых происходит разряд ионов водорода, являются более благородные металлы и другие неметаллические включения. [10]
В связи с неоднородностью поверхности металлов существуют участки, обладающие различной адсорбционной активностью. [11]
 |
Схема электрохимического коррозионного процесса. [12] |
Электрохимическая коррозия возникает в результате неоднородности поверхности металла и образования множества анодных ( с более электроотрицательным потенциалом еа) и катодных ( с более положительным электродным потенциалом ек) участков. [13]
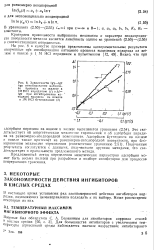 |
Зависимости Igv-IgT при иигибпровании катодного процесса на железе в 1MHCI пиридином ( / и Д ( - IgT при ингибировании катодного процесса на никеле в IM HCI бутиндиолом ( 2. [14] |
Критерием правильности выбранного механизма и характера неоднородности поверхности металла является линейность одного из уравнений (2.50) - (2.55) в соответствующих координатах. [15]
Страницы: 1 2 3