Непостоянство - константа
Cтраница 2
Полученные на основании измерений величины Я, или ос при разных концентрациях константы К несколько изменяются. Непостоянство констант является результатом того, что уравнение Оствальда не учитывает коэффициентов активности, а ими можно пренебречь только для очень разбавленных растворов. Кроме того, истинное значение величины а определяется отношением экспериментально наблюдаемой электропроводности к электропроводности полностью диссоциированного электролита при той концентрации, при которой измерена электропроводность. Для того чтобы определить величину а, нужно найти величину А. [16]
Полученные на основании измерений величины К или а при разных концентрациях константы К несколько изменяются. Непостоянство констант является результатом того, что уравнение Оствальда не учитывает коэффициентов активности, а ими можно пренебречь только в очень разбавленных растворах. [17]
Полученные на основании измерений величины К или а при разных концентрациях константы К несколько изменяются. Непостоянство констант является результатом того, что уравнение Оствальда не учитывает коэффициентов активности, а ими можно пренебречь только для очень разбавленных растворов. Кроме того, истинное значение величины а определяется отношением экспериментально наблюдаемой электропроводности к электропроводности полностью диссоциированного электролита при той концентрации, при которой измерена электропроводность. Для того чтобы определить величину а, нужно найти величину Яионов при данной концентрации по уравнению Кольрауша; ИОНов - о - В У. Эта поправка возникает в связи с изменением подвижности ионов при изменении ионной силы. [18]
Следовательно, превращение азото-8 - одородной смеси - в NH3 в этих условиях происходит с большей полнотой, чем соответствовало бы величине константы равновесия, найденной для низких давлений. Непостоянство константы равновесия, вычисленной оо уравнению ( 6) исходя из величины парциальных давлений, объясняется отклонением реальных газов от состояния идеальных газов. Эти отклонения возрастают с повышением давления. [20]
Необходимо, однако, учитывать, что в разных растительных тканях эти соотношения различны. Непостоянство константы скорости гидролиза гемицеллюлоз растительных тканей осложняет кинетические расчеты. [22]
В противном случае необходимы дополнительные исследования для выяснения причин наблюдаемых расхождений значений констант устойчивости. Одной из причин непостоянства рассчитываемых констант устойчивости может быть образование многоядерных комплексов металла. Изменение констант устойчивости может быть связано и с изменением коэффициентов активности. [23]
Эти особенности проявляются в том, что диссоциация одной формы исшита зависит от его превращения в другую, особенно когда характер связи ионов в обоих формах различен, а также в том, что поглощение ионов, особенно органических, обусловливается не только электростатическим взаимодействием с их ионогеннымя группами, но и адсорбционным взаимодействием неполярных радикалов ионов с поверхностью ионита вблизи ионогенных групп адсорбента за счет молекулярных сил. Обе причины приводят к непостоянству констант ионного обмена. [24]
Постоянство значений к считается весомым аргументом в пользу выбранного уравнения. При этом однако, следует иметь в виду, что непостоянство константы, обусловленное расчетом по неправильному уравнению, должно превышать случайную ошибку, когда для вычисления используют это же уравнение, но являющееся справедливым. Наиболее отчетливо этот критерий проявляется на заключительных фазах кинетической кривой при большой глубине превращения. [25]
Ранее было отмечено, что для растворов сильных электролитов можно пользоваться только понятием кажущейся степени диссоциации. Тогда наблюдающиеся отклонения от закона действия масс, которыми вызвано непостоянство константы диссоциации при разведении, могут быть компенсированы применением таких значений эффективных концентраций, при подстановке которых в выражение константы диссоциации возможно применять закон действия масс к растворам сильных электролитов и к более концентрированным растворам слабых электролитов. Эффективная концентрация называется активностью. [26]
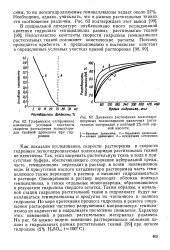
Расчет констант скоростей растворения металлов в органических кислотах показывает, что эти реакции мономолекулярны. Константы некоторых отдельных реакций до некоторой степени удовлетворительно рассчитываются по кинетическому уравнению 1-го порядка; однако в большинстве случаев обнаруживается непостоянство констант, а именно - некоторое их увеличение к концу опыта, что следует из табл. 2, а также из рисунка, где показана логарифмическая зависимость lg ( a - х) от времени t, где а - общее количество растворенного металла за время опыта; х - количество растворенного металла за определенный отрезок времени. [27]
 |
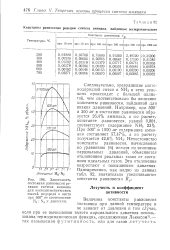
Кинетика установления равновесия при распределении ThB между кристаллами и раствором K2SO4.| Кинетика установления равновесия при распределении радия между кристаллами и раствором K2SO4. [28] |
В частности, было показано, что точка зрения О. Хана в отношении непостоянства константы фракционирования не отвечает действительности. Установлено, что внутриадсорбционное соосаждение радия и свинца на кристаллических осадках сульфата и хромата калия, так же как и процессы захвата, связанные с образованием истинных смешанных кристаллов, могут быть охарактеризованы вполне определенными для данных условий значениями констант фракционирования. [29]
Особенности высокомолекулярных полиэлектролитов заключаются в том, что их способность к диссоциации может быть реализована лишь при замене одного иона на другой, и в том, что на электрохимические явления накладываются явления адсорбционные. Эти особенности проявляются в том, что диссоциация одной формы ионита зависит от его превращения в другую, особенно когда характер связи ионов в обеих формах различен, а также в том, что поглощение ионов, особенно органических, обусловливается не только электростатическим взаимодействием с их ионогенными группами, но и адсорбционным взаимодействием неполярных радикалов ионов с поверхностью ионита вблизи ионогенных групп адсорбента за счет молекулярных сил. Обе причины приводят к непостоянству констант ионного обмена. [30]
Страницы: 1 2 3