Трехвалентный нептуний
Cтраница 1
 |
Абсорбционная характеристика ионов нептуния в водных растворах. [1] |
Трехвалентный нептуний крайне неустойчив к окислению, что затрудняет его получение и исследование. [2]
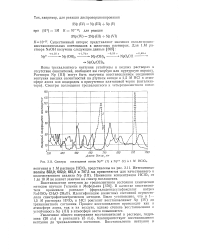 |
Спектры поглощения ионов Np3 ( 1 и Np4 ( 2 в 1 М НСЮ. [3] |
Ионы трехвалентного нептуния устойчивы в водных растворах в отсутствие окислителей, сообщают им голубую или пурпурную окраску. [4]
Растворы трехвалентного нептуния легко приготовить восстановлением нептуния высших валентных состояний на ртутном катоде в инертной атмосфере или водородом с платиновым катализатором. Быстрое окисление трехвалентного нептуния атмосферным кислородом затрудняет получение его солей из водных растворов, особенно в присутствии ионов фторида, оксала-та и гидроксила. [5]
На воздухе трехвалентный нептуний окисляется сначала до четырехвалентного, а затем до пятивалентного. [6]
Реакции осаждения трехвалентного нептуния напоминают реакции редкоземельных элементов, реакции четырехвалентного нептуния напоминают четырехвалентный уран, а реакции нептунила - реакции уранила. Простые соли пятивалентного нептуния растворимы. [7]
Кроме перечисленных окислов, получены еще окись трехвалентного нептуния NpaO3 и закись нептуния NpO, образующаяся при восстановлении двуокиси в токе водорода. [8]
Необходимо отметить, что в табл. 6.4 отсутствуют соединения трехвалентного нептуния. [9]
Соединения Np ( III) изучены меньше, чем соединения других валентных форм нептуния. Трехвалентный нептуний может быть получен электролитическим восстановлением Np ( IV) или Np ( V) на ртутном катоде или восстановлением их водородом на платинированной платине. Под действием кислорода Np ( III) сравнительно быстро окисляется. [10]
Важной характеристикой химических свойств нептуния является относительная устойчивость ( в тех или иных условиях) различных его валентных состояний. Соединения трехвалентного нептуния окисляются на воздухе, а для растворов Np ( V) характерны так называемые реакции диспропор-ционирования, в которых Np ( V) как бы сам себя окисляет и восстанавливает, причем вместо пятивалентного нептуния образуются четырех - и шестивалентный. [11]
Как и все актиноиды, нептуний очень электроположителен. Переход трехвалентного нептуния в четырехвалентный обратим; окисление происходит даже под действием атмосферного водорода. [12]
Растворы трехвалентного нептуния легко приготовить восстановлением нептуния высших валентных состояний на ртутном катоде в инертной атмосфере или водородом с платиновым катализатором. Быстрое окисление трехвалентного нептуния атмосферным кислородом затрудняет получение его солей из водных растворов, особенно в присутствии ионов фторида, оксала-та и гидроксила. [13]
Среди соединений нептуния с галогенами по мере перехода от фтора к иоду убывает прочность соединений с высшими валентностями нептуния. В то время как трехвалентный нептуний Np ( III) дает безводные соединения типа NpX3 со всеми четырьмя галогенами ( F, Cl, Br, J), Np ( IV) уже не дает соли NpJ4, для Np ( V) не выделено соединений с бромом и иодом, a Np ( VI) дает только гексафторид NpF6 - весьма летучее соединение, похожее на гексафторид урана. [14]
Хотя нептуний - элемент искусственный, получены и достаточно хорошо изучены многие его соединения - и обычные, и комплексные. Интересно, что галогениды трехвалентного нептуния внешне совершенно непохожи. Трифторид элемента № 93 - пурпурного цвета, три-бромид - зеленого, трийодид - коричневого, а три-хлорид нептуния бесцветен. [15]
Страницы: 1 2