Нитрат - алюминий
Cтраница 2
Нитрат алюминия легко растворим в воде. Фосфат алюминия нерастворим в воде ( и уксусной кислоте), но растворим в сильных кислотах и щелочах. [16]
Нитрат алюминия Al ( N03) s - 9H20, насыщенный раствор. [17]
Раствор нитрата алюминия имеет дефицит кислоты, равный 1 М, если при добавлении одного моля азотной кислоты на литр этого раствора кислотность его повысится до той, которая образуется при растворении азотнокислого алюминия в воде. [18]
Раствор нитрата алюминия, 1 мл которого равен 1 мг готовят растворением 1 4 г нитрата алюминия в 100 мл воды. [19]
Растворимость нитрата алюминия при 30 С составляет 81 г соли в 100 г воды. [20]
Растворимость нитрата алюминия изменяется от 56 г при 0 С до 120 г А1 ( МО3) з на 100 г Н2О при 80 С. Еще более растворим его перхлорат - 120 г при О С и 180 г А1 ( СЮ4) з на 100 & Н2О при 90 С. [21]
Смесь нитратов алюминия, церия и кадмия, осажденная щелочным фосфатом, к которому добавлен небольшой избыток щелочи, пригодна в качестве катализатора для окисления углеводородов. [22]
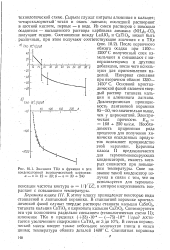 |
Значения ТКе в функции е для. [23] |
Сырьем служат нитраты алюминия и кальция; четыреххлор истыйг титан и окись лантана; последний растворяют в азотной кислоте, первые - в воде. Из смеси растворов с помощью осадителя - насыщенного раствора карбоната аммиака ( NH4) 2 - С03 получают осадок. [24]
Стандартный раствор нитрата алюминия, содержащий 25 мке алюминия в 1 мл. [25]
Девятиводный кристаллогидрат нитрата алюминия легко растворяется в воде и спирте. [26]
Все кристаллогидраты нитрата алюминия, кроме девяти-водного, получаются сравнительно сложными методами. [27]
Для приготовления нитрата алюминия применялась дымящая ( уд. [28]
Применяется раствор нитрата алюминия А1 ( МОз) з или хлорида алюминия А1С13, содержащий 10 мг А1 3 в 1 мл. [29]
Стандартный раствор нитрата алюминия, содержащий 25 мкг алюминия в 1 мл. [30]
Страницы: 1 2 3 4