Нитрат - кальций
Cтраница 3
Нитрат кальция - бедное азотом соединение - обладает плохими физическими свойствами. [31]
Нитрат кальция при комнатной температуре выделяется из водных растворов Ca ( N03) 2 - 4H20 в виде бесцветных кристаллов с температурой плавления 42 7 С. Плавится безводная соль при 561 С; при 500 С начинается ее разложение с выделением кислорода и образованием нитрита кальция. Последний распадается на окись кальция и двуокись азота. Кристаллогидраты и безводная соль гигроскопичны, поэтому нитрат кальция хранят без доступа влаги. [32]
Нитрат кальция получается нейтрализацией слабой азотной кислоты известняком или мелом и при поглощении хвостовых нитроз-ных газов, отходящих от производства азотной кислоты, известковым молоком. [33]
Нитрат кальция 7 5 % - ный водный раствор. [34]
Нитрат кальция, Ca ( N03) 2 - яН20 ( п0, 2, 3 и 4) встречается в природе в виде норвежской селитры. [35]
Нитрат кальция применяют в сельском хозяйстве в качестве удобрения под ячмень, овес, коноплю и картофель. [36]
Нитрат кальция Са ( N03) 2 iIIaO получают действием разбавленной азотной кислоты на чистый ирепарат карбоната кальция. Для этого присыпают исходную соль пеболыпидш порциями к кислоте до тех пор, пока она не перестанет растворяться. Полученный раствор фильтруют и, слегка аодкислив, осторожно упаривают при температуре не выше 40 С до начала кристаллизации. Выпавшие при охлаждении бесцветные кристаллы нитрата отсасывают, отжимают между листами фильтровальной бумаги и сушат непродолжительное время в эксикаторе пад едким кали. [37]
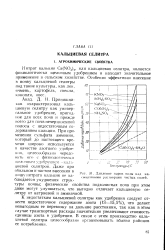 |
Давление паров воды над насыщенными рас. порами чистых солей. [38] |
Нитрат кальция Ca ( NO3) 2, или кальциевая селитра, является физиологически щелочным удобрением и находит значительное применение в сельском хозяйстве. Особенно эффективно внесение в почву кальциевой селитры под такие культуры, как лен, ячмень, картофель, свекла, конопля, овес. [39]
Нитрат кальция Са ( МО3) г - 4Н2О получают действием разбавление и азотной кислоты на чистый прегарат карбоната кальция. Для этого присыпают исходную соль небольшими порциями к кислоте до тех пор, пока сна не перестанет растворяться. Полученный раствор фильтруют и, слегка пэдкислив, осторожно упаривают при температуре не выше 40 до начала кристаллизации. Выпавшие при охлаждении бесцветные кристаллы нитрата отсасывают, отжимают между листами фильтровальной бумаги и сушат непродолжительное время Б эксикаторе над едким кали. [40]
Нитрат кальция Са ( МОз) 2, или кальциевая селитра, получается в больших количествах нейтрализацией азотной кислоты известью; применяется как удобрение. [41]
Нитрат кальция Ca ( NO3) 2, или кальциевая селитра, также используется в качестве удобрения. Получают его, нейтрализуя азотную кислоту гидроксидом Са ( ОН) 2 или карбонатом кальция СаСО3; содержит 13 % ( мае. [42]
Нитрат кальция Са ( МО3) з, тривиальное название кальциевая, или известковая, селитра, обычно кристаллизуется из воды в виде кристаллогидрата Са ( ЫОзЬ-4Н2О. [43]
Нитрат кальция Ca ( NO3) 2 изготовляется в виде продуктов, состоящих из бесцветных, растворимых в воде кристаллов состава Ca ( NO3) 2 4Н2О, расплывающихся на воздухе, и различных примесей. Он поставляется в расфасованном виде в барабанах и мешках, должен храниться в сухом закрытом складе. Применяется в качестве ускорителя, антифриза, а также ингибитора. [44]
Нитрат кальция Са ( NO3) 2 - 4H2O - прозрачные призматические кристаллы, расплывающиеся на воздухе. Соль плавится при 42 5 С. Безводная соль нитрата кальция - белый порошок, получается при нагревании кристаллогидрата до 170 С. [45]
Страницы: 1 2 3 4