Нитрат - щелочной щелочноземельный металл
Cтраница 1
Нитраты щелочных и щелочноземельных металлов в водных растворах имеют нейтральную реакцию. [1]
Из табл. 2.1 видно, что нитраты щелочных и щелочноземельных металлов разлагаются со значительным поглощением тепла: это отражается, конечно, на общем тепловом балансе изготовленных с их участием составов. [2]
Соли азотной кислоты называются нитратами, а нитраты щелочных, щелочноземельных металлов и аммония называют еще селитрами - калийная селитра, аммонийная селитра. [3]
Бок [94, 96] для высаливания Тп ( МОз) 4 в диэтиловый эфир при применении нитратов щелочных и щелочноземельных металлов, объясняется тем, что они использовали насыщенные растворы различных нитратов и, таким образом, имели совершенно различные моляльности нитратов в каждой системе. [4]
Если приведенные выше представления справедливы, то надо было бы ожидать, что напряжение разложения нейтральных растворов таких солей, как сернокислый натрий и вообще сульфаты и нитраты щелочных и щелочноземельных металлов, должно было бы равняться примерно 1 7 в, но в действительности соответствующие значения заметно больше. Однако необходимо помнить, что так как эти растворы не буферные, то в результате разряда ионов водорода раствор вблизи катода подщелачивается, тогда как при разряде ионов гидроксила раствор у анода подкисляется. Следовательно, разряд ионов водорода происходит из более щелочного, а ионов гидроксила из более кислого раствора по сравнению с раствором в слоях, удаленных от электродов; поэтому напряжение разложения здесь больше 1 7 в. Эта последняя величина имела бы место, если бы оба иона разряжались из одного и того же раствора. [5]
Другой метод, целью которого является получение Sr90 и Cs137, состоит в том, что жидкие стоки выпаривают до тех пор, пока они не станут твердыми; остаток нагревают до 300 С с тем, чтобы все нитраты щелочных и щелочноземельных металлов перешли в нерастворимые окислы. Затем твердый остаток экстрагируется водой, при этом изотопы стронция и цезия переходят в раствор. Этот раствор концентрируется для хранения на складе, тогда как экстрагированный остаток теряет свою радиоактивность в сравнительно короткое время. [6]
Определению хрома ( VI) в присутствии маскирующего реагента - нитрилотриметилфосфоновой кислоты - не мешает 100-кратное содержание Feni, Сгш, WVI, 1000-кратное содержание Со, V, 1 - 10 мг ионов Си, Ni, а также 0 05 - 0 20 г сульфатов, фосфатов, хлоридов, ацетатов, нитратов щелочных и щелочноземельных металлов, марганца и свинца. В присутствии 1 М растворов хлоридов, сульфатов, нитратов щелочных металлов скорость каталитической реакции увеличивается вдвое, а некаталитической - в 1 5 раза. Реакция окисления о-аминофенола пероксидом водорода применена для анализа неорганических веществ особой числоты. [7]
Укрепить ее в штативе вертикально над металлической подставкой и нагревать до расплавления соли. Нитраты щелочных и щелочноземельных металлов, плавясь, разлагаются на нитриты и кислород. [8]
Ход реакций разложения нитратов при нагревании зависит от поляризующего действия иона металла. Так, при разложении нитратов щелочных и щелочноземельных металлов образуются соответствующие нитриты и кислород. Нитраты металлов с большим ионным, потенциалом разлагаются на оксид металла, NOg и кислород. [9]
Практическое значение получили элементы, содержащие электролит, температура плавления которого не выше 600 С. Это обычно смесь хлоридов, бромидов и нитратов щелочных и щелочноземельных металлов. В качестве анодов рекомендуют применять кальций, магний и сплавы лития. Катоды выполняют из серебра, меди, никеля и железа. Поверхность их покрыта деполяризатором, который иногда добавляется также непосредственно в электролит. [10]
Метод основан на измерении светопоглощения нитрат-ионов в кислом растворе при Х 302 нм. Метод применим для анализа растворов азотной кислоты, смесей нитратов щелочных и щелочноземельных металлов. [11]
По способу Бухнера ( Nuvalonverfahren) отделение А1203 от Si02, Fe203 и Ti02 достигается нагреванием глины в автоклаве с азотной кислотой, соответствующей концентрации и в необходимом количество. Нитрат алюминия, переходящий в раствор, загрязнен в основном только нитратами щелочных и щелочноземельных металлов, от которых его можно отделить фракционной кристаллизацией. Азотная кислота выделяется при термическом разложении водного нитрата алюминия, и А12О3 получается в очень чистом состоянии. По способу Голъдшмидта ( Goldschmidt) для вскрытия используют водный раствор значительно более дешевой сернистой кислоты. При этом в большинстве случаев в раствор переходят значительные количества железа, которое, однако, образует с алюминием хорошо кристаллизующуюся основную соль; до тех пор пока количество железа не слишком велико, возможно сравнительно простое отделение алюминия путем фракционной кристаллизации основного сульфита. [12]
По способу Бухнера ( Nuvalqnyerfahren) отделение А12О3 от Si02, Fe2O3 и TiO2 - достигается нагреванием глины в автоклаве с азотной кислотой, соответствующей концентрации и в необходимом количестве. Нитрат алюминия, переходящий в раствор, загрязнен в основном только нитратами щелочных и щелочноземельных металлов, от которых его можно отделить фракционной кристаллизацией. Азотная кислота выделяется при термическом разложении водного нитрата алюминия, и А12О3 получается в очень чистом состоянии. При этом в большинстве случаев в раствор переходят значительные количества железа, которое, однако, образует с алюминием хорошо кристаллизующуюся основную соль; до тех пор пока количество железа не слишком велико, возможно сравнительно простое отделение алюминия путем фракционной кристаллизации основного сульфита. [13]
По способу Бухнера ( Niavalonverfahren) отделение А1203 от Si02, Fe203 и TiOg достигается нагреванием глины в автоклаве с азотной кислотой, соответствующей концентрации и в необходимом количестве. Нитрат алюминия, переходящий в раствор, загрязнен в основном только нитратами щелочных и щелочноземельных металлов, от которых его можно отделить фракционной кристаллизацией. Азотная кислота выделяется при термическом разложении водного нитрата алюминия, и А1203 получается в очень чистом состоянии. По способу Голъдшмидта ( Goldschmidt) для вскрытия используют водный раствор значительно более дешевой сернистой кислоты. При этом в большинстве случаев в раствор переходят значительные Количества железа, которое, однако, образует с алюминием хорошо кристаллизующуюся основную сольдо тех пор пока количество железа не слишком велико, возможно сравнительно простое отделение алюминия путем фракционной кристаллизации основного сульфита. [14]
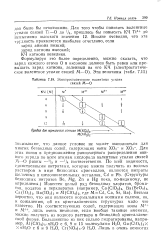 |
Электростатические валентные усилия связей М - О. [15] |
Страницы: 1 2