Нитрат - палладий
Cтраница 1
Нитрат палладия ( П) Pd ( NOj) a образует желто-коричневые гигроскопичные кристаллы. [1]
Нитрат палладия не рекомендуется применять в качестве реактива, потому что он с анионом бромистоводородной кислоты образует буровато-красный осадок. [2]
Нитрат палладия ( II) образуетстио-сульфатом натрия темно-коричневый комплекс, который очень легко может быть количественно экстрагирован метиленхлори дом после добавления, например, ацетата трибутиламмония. [3]
Из раствора, например гидролизом нитрата палладия ( П), получают гидроокись палладия Pd ( OH) 2 или гидратированную окись палладия, окрашенную в бурый цвет и растворяющуюся в кислотах. Содержание воды в ней колеблется; при нагревании постепенно происходит обезвоживание, причем цвет становится черным и теряется растворимость в кислотах. [4]
Количественно осаждается также при кипячении нитрата палладия с азотной кислотой, броматом натрия и азотнокислой ртутью. [5]
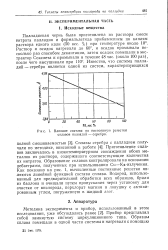 |
Влияние состава на постоянную решетки сплавов палладий - серебро. [6] |
Палладиевая чернь была приготовлена из раствора смеси нитрата палладия и формальдегида прибавлением по каплям раствора едкого кали ( 50 вес. [7]
Катализаторами являются смесь хлоридов палладия и меди, нитрат палладия и особенно ТеО2, промотированный соединениями брома. Синтез ведут при 160 С и ж 2 8 МПа с 60 % - ной степенью конверсии этилена и циркуляцией непревращенных газов. Вторая стадия заключается в гидролизе полученной смеси водой при ПО-130 С, когда вырабатывают уксусную кислоту, направляемую на рециркуляцию, и этиленгликоль. При этом суммарный выход этилен-гликоля достигает 94 % по этилену, что значительно превосходит традиционный способ синтеза. Сообщается о пуске крупных установок производства этиленгликоля по этому методу, но надежных данных по технологии и экономике производства пока нет. [8]
При добавлении капли 1 % - ного раствора нитрата палладия к капле раствора мочевины осадок не появляется, но при последующем прибавлении небольшого количества хлорида или бромида натрия образуются кристаллы-желтые ромбы и линзы, часто собранные в розетки. Тиомочевина при этой реакции образует осадок, кристаллизующийся в форме бурых дендритов, ромбов, игл. [9]
Достаточно высокий выход щавелевой кислоты достигается при использовании в качестве катализатора нитрата палладия. [10]
В капиллярном конусе к 50 нл раствора смеси солей прибавляют 100 нл свежеприготовленного 2 % - ного раствора нитрата палладия и центрифугируют. [11]
Оксид палладия ( РсЮ) используется как редукционный катализатор в синтезе органических соединений. Нитрат палладия ( Pd ( NO3) 2) используется для разделения галидов. [12]
Индикатор приготовляют растворением нитрата палладия ( II) ( в количестве, отвечающем содержанию 0 06 г палладия) в 100мл 16 % - яой азотной кислоты. При добавлеш: и 0 25 мл такого раствора к 10 мл воды, содержащей 0 007 мг иодид-ионоз ( концентрация - 0 7 мг / л или приблизительно 5 - 10 - 6 М), получается заметное окрашивание. Когда в растворе имеется осадок иодида серебра, чувствительность индикатора равна только 2 мг / л нодид-ионов. [13]
Для выделения палладия по этому методу солянокислый раствор платиновых металлов выпаривают до небольшого объема, добавляют 25 мл концентрированной HNO3 и в закрытом стакане емкостью 250 мл нагревают на плитке почти до кипения; нагревание продолжают до прекращения выделения бурых паров, которые образуются от взаимодействия азотной и соляной кислот и разложения нестойких хлоридов. В конце этой стадии большая часть палладия выделяется в виде темных красновато-коричневых кристаллов безводного хлористого палладия, быстро осаждающихся на дно. Стакан снимают с плитки и, не охлаждая, отстоявшуюся жидкость возможно полнее сливают декантацией в другой такой же стакан; кристаллы промывают четыре раза небольшими порциями по 2 - 3 мл концентрированной HN03, присоединяя промывные жидкости к первому основному раствору. Если несколько кристаллов будет увлечено промывной жидкостью при декантации, то это не вызовет затруднений в дальнейшем ходе анализа. Стакан с жидкостью, полученной от декантации, закрывают, помещают на электрическую плитку и добавляют 5 капель концентрированной НС1 для переведения в хлорид небольших количеств нитрата палладия, образовавшегося при первом выпаривании; нагревают почти до кипения. После удаления бурых паров сильнокислый раствор хорошо охлаждают, погрузив нижнюю часть стакана в холодную воду. Отстоявшуюся жидкость под небольшим вакуумом декантируют через стеклянный тигель с пористым дном; кристаллы хлористого палладия промывают четыре раза порциями по 3 мл охлажденной концентрированной HNO3, сливая промывные жидкости через фильтр-тигель. [14]
Страницы: 1