Чистый нитрат - аммоний
Cтраница 1
Чистый нитрат аммония неспособен к самораспространяющемуся горению на воздухе. [1]
Чистый нитрат аммония плавится при 169 6 С. [2]
Чистый нитрат аммония может взорваться вследствие детон-тации, вызванной взрывом какого-либо сильновзрывчатого ( инициирующего) вещества-детонатора. Для осуществления такого взрыва детонатор должен быть взят в определенном количестве, чтобы вызвать мощную взрывную волну большой скорости. [3]
Чистый нитрат аммония не чувствителен к ударам или трению, но при определенных условиях обладает взрывчатыми свойствами. Вследствие этого его используют и как сырье для производства аммонийно-селитренных взрывчатых веществ - аммонитов ( смесей NH4NO3 с древесной мукой и другими органическими материалами с добавкой нитропродуктов), аммоналов ( смесей, содержащих алюминиевый порошок) и др. Они взрываются только от детонатора. Взрывы чистой аммонийной силитры могут быть вызваны термическим разложением соли в замкнутом пространстве. При этом газообразные продукты разложения ( NO2) служат катализаторами дальнейшего разложения, приводящего к взрыву. Взрывоопасность NH4NO3 возрастает в присутствии минеральных кислот и легко окисляющихся примесей ( смазочных масел и др.) и уменьшается при увеличении влажности соли. Для предотвращения самопроизвольного разложения к ней добавляют стабилизаторы - вещества, связывающие образующуюся при разложении азотную кислоту и Г Ю2 или выделяющие при взаимодействии с NH4NO3 аммиак, который нейтрализует азотную кислоту и восстанавливает оксиды азота до элементарного азота. [4]
 |
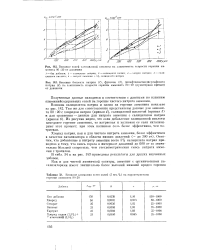
Растворимость MHNO3 в воде. [5] |
Чистый нитрат аммония плавится при 169 6 С. [6]
Чистый нитрат аммония не чувствителен к ударам или трению, но при определенных условиях обладает взрывчатыми свойствами. Вследствие этого его используют и как сырье для производства ам-миачно-селитренных взрывчатых веществ - аммонитов ( смесей NH4NO3 с древесной мукой и другими органическими материалами с добавкой нитропродуктов), аммоналов ( смесей, содержащих алюминиевый порошок) и др. Они взрываются только от детонатора. Взрывы чистой аммиачной селитры могут быть вызваны, помимо воз-действия детонаторов, термическим разложением соли в замкнутом пространстве. При этом газообразные продукты разложения ( NO2), по-видимому, служат катализаторами дальнейшего разложения, приводящего к взрыву. Взрывоопасность NH4NO3 возрастает в присутствии минеральных кислот и легко окисляющихся материалов и уменьшается при увеличении влажности соли. При содержании больше 3 % воды аммиачная селитра не взрывается даже при взрыве детонатора. Для предотвращения самопроизвольного разложения к ней добавляют стабилизаторы - вещества, связывающие образующуюся при разложении азотную кислоту и NO2 или выделяющие при взаимодействии с NH4NO3 аммиак, который нейтрализует азотную кислоту и восстанавливает оксиды азота до элементарного азота. [7]
Чистый нитрат аммония может взорваться вследствие детонации, вызванной взрывом какого-либо сильновзрывчатого ( инициирующего) вещества - детонатора. [8]
 |
Характеристика кристаллических модификаций нитрата аммония. [9] |
В зависимости от температуры чистый нитрат аммония существует в различных кристаллических модификациях ( табл. VII. Превращение одних кристаллических форм в другие сопровождается - изменением структуры и плотности кристаллов и протекает с выделением тепла. [10]
Полученные данные находятся в соответствии с данными по влиянию алюминийсодержащих солей на горение чистого нитрата аммония. [12]
 |
Влияние химической природы горючего на зависимость скорости горения стехиометрических смесей на основе нитрата аммония от давления. [13] |
Таким образом, уголь сгорает менее полно, чем аммиак, следовательно, как и при горении чистого нитрата аммония, добавки катализируют в первую очередь окисление аммиака. [14]
В результате образования KNO3 - сухой, почти не гигроскопичной соли-получаемый продукт приобретает лучшие физические свойства, чем чистый нитрат аммония. [15]
Страницы: 1 2