Нитрат-ионы
Cтраница 1
Нитрат-ионы обнаруживают реакцией с дифениламином, который в среде концентрированной серной кислоты с МО3 - - ионами дает синее окрашивание. Реакция с дифениламином чувствительная, но не характерная, так как синее окрашивание возникает и в присутствии хромат-ионов. [1]
Нитрат-ионы с этим реактивом не дают окрашивания. Сильные окислители разрушают реактив, поэтому мешают выполнению реакции. В присутствии в анализируемом растворе ионов трехвалентного железа, мешающих реакции, необходимо перед обнаружением нитрит-ионов прибавить к раствору немного винной кислоты или фторида натрия для связывания в комплекс ионов железа. [2]
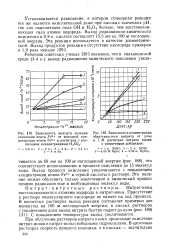 |
Зависимость выходов реакции окисления ионов Fe2 от исходной концентрации ионов Fe2 в растворах с различными концентрациями H2SO4.| Зависимость концентрации. [3] |
Нитрат-ионы восстанавливаются атомами водорода в нитрит-ионы. Присутствие в растворе молекулярного кислорода не влияет на ход процесса. В щелочных растворах выход реакции составляет примерно две молекулы на 100 эв поглощенной энергии; в кислых растворах с увеличением дозы выход нитрита быстро падает до нуля ( рис. 189) [31] С повышением температуры выход увеличивается. [4]
Нитрат-ионы являются анионами азотной кислоты, одной из самых сильных минеральных кислот. Она является сильным окис-лителем, окисляющим многие восстановители. Азотную кислоту широко используют в анализе для растворения металлов и сплавов, сульфидов и других соединений. Нитраты - соли азотной кислоты - хорошо растворяются в воде, кроме основных солей висмута и ртути. [5]
Нитрат-ионы часто мешают последующему определению рения. При спектрофотометрических определениях они окисляют восстановитель и рений в степени окисления менее семи, осаждаются при весовом определении, соэкстрагируются при экстракционно-фотометрическом и флуориметрическом определениях. Для отделения или уменьшения концентрации нитрат-ионов растворы выпаривают до небольшого объема ( 1 - 2 мл) на водяной бане или нагретом блоке с температурой 110 С; более полное удаление нитрат-ионов достигается при многократном выпаривании растворов с соляной кислотой. Показана возможность применения для этой цели выпаривания с серной кислотой до начала выделения ее паров. Иногда рекомендуют применять методы ионообменной хроматографии. [6]
Нитрат-ионы можно определять прямым спектрофотометрическим методом, измеряя оптическую плотность раствора при длине волны 302 нм. Катионы металлов отделяют пропусканием анализируемого раствора через колонку с Н - катионитом. В результате ионного обмена 2RH Ме2 RzMe 2Н в раствор переходит эквивалентное количество ионов водорода, причем образовавшиеся кислоты ( НС1, Нг8О4, НС1О4) не мешают определению нитрат-ионов указанным методом. [7]
Нитрат-ионы образуют с бруцином сначала соединение красного цвета, но затем окраска быстро изменяется на желтую, сильно поглощающую в области 400 - 410 нм. Наилучшие результаты получаются в диапазоне 1 - 4 мкг / мл, когда кривая поглощение-концентрация N03 близка к линейной. [8]
Нитрат-ионы также адсорбируются осадком. Поэтому, если раствор после озоления азотнокислый, нитрат-ионы удаляют путем выпаривания аликвотной части раствора досуха и трехкратной обработки его раствором концентрированной соляной кислоты с последующим выпариванием. [9]
Нитрат-ионы можно определять прямым спектрофотометрическим методом, измеряя оптическую плотность раствора при длине волны 302 нм. Катионы металлов отделяют пропусканием анализируемого раствора через колонку с Н - катионитом. В результате ионного обмена 2RH Ме2 Е R2Me 2H в раствор переходит эквивалентное количество ионов водорода, причем образовавшиеся кислоты ( НС1, FhSOi, HClOi) не мешают определению нитрат-ионов указанным методом. [10]
Нитрат-ионы можно определять прямым спектрофотометрическим методом, измеряя оптическую плотность раствора при длине волны 302 им. Катионы металлов отделяют пропусканием анализируемого раствора через колонку с Н - катионитом. В результате ионного обмена 2RH Ме2 F R2Me 2H в раствор переходит эквивалентное количество ионов водорода, причем образовавшиеся кислоты ( НС1, HaSO4, HClO / j) не мешают определению нитрат-ионов указанным методом. [11]
Нитрат-ионы и ионы калия, как однозарядные ионы, во всех случаях не способны вызвать коагуляцию белковых макромолекул. [12]
Нитрат-ионы являются анионами азотной кислоты-одной из самых сильных минеральных кислот. Она является сильным окислителем, окисляющим многие восстановители. Азотную кислоту широко используют в анализе для растворения металлов и сплавов, сульфидов и других соединений. Нитраты-соли азотной кислоты - хорошо растворяются в воде, кроме основных солей висмута и ртути. [13]
Нитрат-ионы и более чем 10 000-кратные количества сульфат-ионов не влияют на нее, но иодиды очень сильно искажают ее ход. При одновременном присутствии трех галогенидов рекомендуется их ионообменное разделение, но иод можно независимо определить в отдельной порции раствора с помощью иодоселек-тивного электрода. [14]
Нитрат-ионы, которые также участвуют в переносе электричества, не изменяются и не уничтожаются при электролизе. Они лишь накопляются в ано-лито, где должно находиться такое же количество ионов серебра, чтобы раствор в целом остался электронейтральным. [15]
Страницы: 1 2 3 4