Нитрид - кобальт
Cтраница 1
Нитриды кобальта лучше всего получать азотирона-нисм пирофорного кобальта, который отличается большой активностью. В связи с этим удобно проводить реакцию получения металла и реакцию азотирования последовательно, в одном приборе. [1]
Нитрид кобальта лучше всего получать азотированием пирофорного кобальта, который отличается большой активностью. В связи с этим удобно проводить реакцию получения металла и реакцию азотировачия последовательно, в одном приборе. [2]
Нитрид кобальта Co2N получен действием аммиака на металлический кобальт при температуре 380 С или разложении CoF2 в атмосфере аммиака. [3]
Нитриды кобальта лучше всего получить азотированием пирофорного кобальта, который отличается большой активностью. [4]
Нитрид кобальта, CoN, получают нагреванием ( 40 - 50) Co ( NH2) 3; он представляет собой пирофорный черный аморфный порошок, который растворяется в щелочах с выделением аммиака и в разб. [5]
Нитриды кобальта лучше всего получить азотированием пирофорного кобальта, который отличается большой активностью. [6]
Нитрид кобальта Co2N серовато-черного цвета, хранить его следует в запаянной ампуле. По имеющимся данным, состав продуктов несколько отклоняется от точно теоретического. [7]
Полученный нитрид кобальта Co2N имеет серовато-черный цвет, хранить его следует в запаянной ампуле. [8]
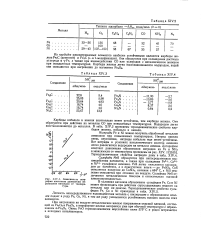 |
Зависимость логарифма константы равновесия образования нитридов от температуры. [9] |
Нитрид никеля очень неустойчив, нитриды кобальта еще менее устойчивы. Все нитриды в условиях каталитического синтеза аммиака легко разлагаются водородом на металл и аммиак. Логарифмы констант равновесия образования нитридов из Fe и NHa в зависимости от температуры приведены на рис. XIV. Термодинамические свойства нитридов даны в табл. XIV.4. Сульфиды MeS образуются при непосредственном взаимодействии элементов, а также при осаждении Fe2, Co2 и Nia сульфидом аммония. CoS окисляется воздухом до CoSO4, начиная с 684 С, a NiS медленно окисляется при стоянии на воздухе. Сульфиды MeS отличаются металлическим блеском и относительно высокой электропроводностью. [10]
Он медленно растворяется в разбавленных минеральных кислотах ( потенциал пары Со2 / Со составляет - 0 277 в), но обладает сравнительно низкой реакционной способностью. Кобальт не соединяется непосредственно с водородом и азотом, и, по-видимому, гидрид и нитрид кобальта вообще не существуют. При нагревании металл вступает в реакции с углеродом, фосфором и серой. [11]
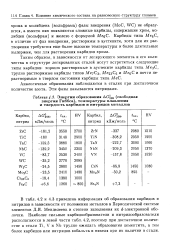 |
Энергии образования AGjgg ( свободная. [12] |
В табл. 4.2 и 4.3 приведена информация об образовании карбидов и нитридов в зависимости от положения металлов в Периодической системе элементов Д.И. Менделеева и степени заполнения их d - электронной оболочки. Наиболее сильные карбидообразователи и нитридообразователи располагаются в левой части табл. 4.2, поэтому при достаточном количестве в стали Ti, V и Nb трудно ожидать образования цементита, а тем более карбидов или нитридов кобальта и никеля при их наличии в стали. [13]
При сильном нагревании химическая активность кобальта возрастает. При сплавлении он реагирует с углеродом, кремнием, серой с образованием карбидов, силицидов и сульфидов. Гидриды и нитриды кобальта получены косвенным путем. [14]
Страницы: 1