Нноз
Cтраница 1
ННОз должно быть близко к 1 7 вольта, если перенапряже ние кислорода считать равным 0 45 вольта. [1]
ННОз при комнатной температуре в течение 1 - 2 мин. [2]
ННОз по 5 - 7 мл в каждый стакан, накрывают часовым стеклом. После растворения пробы в стакан доливают около 10 мл дистиллированной воды и пробу количественно переносят в колбу вместимостью 50 мл, обмывая стакан небольшими порциями дистиллированной воды. После приготовления растворов включают и настраивают прибор. Примесь определяют, используя соответствующую лампу с полым катодом. [3]
Если полученный раствор подкислить ННОз или, еще лучше, НС1, то, как подробно рассмотрено в § 46, произойдет разрушение комплекса [ AgNH3) 2 ] и AgCI снова выпадет в осадок. [4]
Отвешивают порцию выделенного теллура и растворяют в ННОз при нагревании. Раствор после разбавления водой оставляют на 12 час. Раствор подкисляют НЫОз, вссстанавливают JO до J2 солянокислым гидроксиламином и иод экстрагируют ССЦ. Проводят еще две экстракции. Время этих операций должно быть минимальным: оно определяет момент отделения иода от материнского теллура. Органическую фазу обрабатывают раствором NaHSOa до обесцвечивания обеих фаз. Проводят еще три экстракции иода после обработки водных растворов конц. На последней стадии из водного раствора осаждают AgJ; осадок обрабатывают при нагревании HNO3 ( 1: 1), центрифугируют, промыт вают водой и спиртом, высушивают при 110 С. [5]
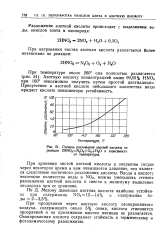 |
Степень разложения азотной кислоты по. [6] |
Азотную кислоту концентрацией выше 99 55 % ННОз при 160 невозможно получить путем простой дистилляции. Присутствие в азотной кислоте небольшого количества воды придает кислоте повышенную устойчивость. [7]
Железистосинеродистый калий, 5 % - ный раствор, подкисленный ННОз ( на 100 мл раствора 1 мл азотной кислоты уд. [8]
Расставим коэффициенты в реакции взаимодействия магнитного железняка с концентрированной - ННОз. Метод сводится к следующему. [9]
Одноосновная к-та, более сильная, чем уксусная, При действии на нее дымящей ННОз образуется 5-нитробарбитуровая к-та, при р-ции с HNO2 - виолуровая, при алкилиро-вапии диметилсульфатом - 1 3-диметилбар-битуровая. [10]
Осадок 3 промывают на фильтре горячей водой и затем обрабатывают на фильтре же разбавленной ННОз, при этом железо переходит в раствор в виде Ре ( МО3) з, а Н МпОз остается на фильтре. [11]
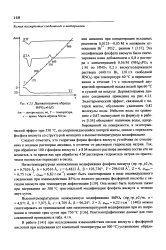 |
Дериватограмма образца. [12] |
Эта модификация фосфата висмута была синтезирована нами добавлением к 0 8 л раствора с концентрацией 0 56 М ( МИЦ) зРО4 и 1 М по НМОз 0 2 л висмутсодержащего раствора ( 440 г / л Bi, 120 г / л свободной ННОз) при температуре 60 С и перемешивании в течение 1 ч с последующей двукратной промывкой осадка водой при 60 С и сушкой на воздухе. Дериватограмма данного соединения приведена на рис. 4.23. Эндотермический эффект, связанный с потерей массы, обусловлен удалением 0 82 молекулы воды. Избыток воды по сравнению с 0 67 молекулами на формулу в работе [134] объясняют наличием воды, адсорбированной на поверхности, а экзотермический эффект при 550 С, не сопровождающийся потерей массы, связан с переходом фосфата висмута со структурой монацита в высокотемпературную модификацию. [13]
В обычных условиях устойчив к ДЕЙСТВИЮ О и влаги, реаг. HCl-кислотой я HsSO; царская водка и ННОз пассивируют X. [14]
В кислотах, не обладающих окислительными свойствами ( например, в НС1), сталь, а тем более чугун, очень сильно разрушаются. В кислотах с окислительными свойствами ( H2SO4, ННОз) на поверхности железа образуются защитные пленки, препятствующие дальнейшей коррозии. Это относится к сравнительно концентрированным кислотам. Так, НМОз при концентрации более 30 % пассивирует железо, а при концентрации выше 50 % практически не действует на него. [15]
Страницы: 1 2