Атомный номер - элемент
Cтраница 1
Атомный номер элемента уменьшается на единицу, а масса ядра остается практически неизменной. Так калий превращается в аргон. [1]
Атомный номер элемента соответствует числу электронов в атоме, период - числу оболочек, а группа - числу электронов на последней оболочке, соответствующей наибольшей энергии электронов для данного атома ( наибольшее число п), эти электроны носят название валентных электронов. [2]
Атомный номер элемента Z, входящий в эту формулу, равен числу электронов в нейтральном атоме. С другой стороны, аа, как уже указывалось, имеет размерность площади. [3]
И фактически атомные номера элементов определяются величиной положительного заряда их ядер / а не количеством электронов; поскольку число последних может легко меняться, приводя к образованию ионов, а для изменения количества протонов в ядре требуется много энергии. [4]
Определить атомный номер Z элемента, у которого длина волны линии La равна 0 131298 нм. [5]
Чем больше атомный номер элемента, тем короче длины волн соответствующих линий рентгеновского спектра, поскольку больший заряд ядра обусловливает более прочную связь внутренних электронов в атоме. [6]
Определить атомный номер Z элемента, у которого длина волны линии La равна 0 131298 нм. [7]
Определить атомный номер Z элемента, у которого длина волны линии / С равна 0 19399 нм. [8]
При увеличении атомного номера элемента уменьшается изотопический сдвиг в спектре ИК поглощения молекул. Поэтому при использовании описываемого ниже метода прямой ИК многофотонной диссоциации молекул, содержащих такие элементы, получают малый коэффициент разделения. В этом случае оказывается более выгодным использовать ИК излучение умеренной интенсивности только для предварительного изотонически-селективного возбуждения, а диссоциацию осуществлять УФ лазерным источником. [10]
Столбец 1 - Атомный номер элемента, равный заряду ядра атома, Столбец 2 - Устойчивые и - радиоактивные ядра. [11]
На распределение влияет атомный номер элементов, из которых состоит мишень. По этой причине следует различать случаи легких ( Z6), промежуточных ( 6 Z 30) и тяжелых ( Z 30) элементов. [12]
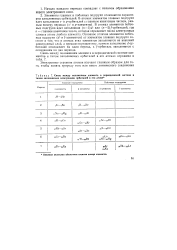 |
Связь между положением элемента в периодической системе и типом заполняемых электронами орбиталей в его атоме. [13] |
Нижними индексами обозначены атомные номера элементов. [14]
Массовое число и атомный номер элемента ( число протонов) обозначают числовыми индексами слева от символа химического элемента; верхний индекс означает массовое число, нижний - заряд ядра. [15]
Страницы: 1 2 3 4