Нейтральный носитель
Cтраница 1
Нейтральные носители имеют или образуют при комп-лексообразовании с катионами тороидальную структуру, имеющую как полярные связи, ориентированные в центр оболочки, так и неполярные - вне ее, что приводит к ли-пофильности всей структуры. Стабильность комплексов с различными катионами зависит от структуры лиганда, размера катиона и минимального размера полости внутри лиганда, что и обуславливает высокую селективность комплексообразования. [1]
Пленочный вариант ИСЭ содержал нейтральный носитель, о-нит-рофенил-н - октиловый эфир и тетрафенилборат натрия. [2]
Осадочные хроматограммы могут быть получены при использовании нейтральных носителей и на фильтровальной бумаге. [3]
В насадочных колонках жидкость наносится на поверхность твердого нейтрального носителя, обладающего макропористостью. Размеры частиц составляют 0 25 - 0 5 мм. В качестве носителей используется инзенский, дмитровский или диатомитовый кирпич. Для нанесения жидкую фазу растворяют в метаноле или ацетоне, которые затем испаряют. Носитель, покрытый жидкостью, является сыпучим, и заполнение им колонок производится так же, как и твердым сорбентом. Капиллярные колонки заполняются растворенным жидким сорбентом, для проталкивания его через капиллярную трубку используется избыточное давление. После заполнения растворитель испаряют. [4]
В [153] также описывается рСа - ИСЭ на нейтральном носителе - аналоге аммановского лиганда. [5]
Для композиции, назначение которой определяется только активным началом, а другие компоненты являются нейтральными носителями, допускается указание только активного начала и его количественного содержания в составе композиции. [6]
В качестве носителя для катализатора лучше всего применять кислые соединения, так как при использовании нейтральных носителей, например активированного угля, могут образоваться алкил-фосфаты, которые затем улетучиваются. [7]
Для композиций, назначение которых определяется только новым активным началом, а другие компоненты являются нейтральными носителями из круга традиционно применяющихся в композициях этого назначения, допускается указание в формуле только этого активного начала и его количественного содержания в составе композиции. [8]
Электрофорез белков в жидкой среде имеет как преимущества, так и недостатки по сравнению с электрофорезом на нейтральных носителях. [9]
Как показал анализ литературы, наиболее пригодными для этой цели могут яв-иться катализаторы на основе окислов металлов V группы и металлов II группы, нанесенных на нейтральные носители, содержащие элементы III и IV групп. [10]
Непрореагировавший малеиновый ангидрид гидролизуется в; водном растворе и дает матрицу полианионной природы. Широко применяемые в настоящее время нейтральные носители типа, сефарозы или биогеля не обладают такими анионными свойствами. Сополимер этилена и малеинового ангидрида выпускается. [11]
На рис. 7.3 приведена схема классификации ИСЭ. Среди этих ИСЭ наибольший интерес представляет ИСЭ на основе нейтральных носителей или, как их еще называют, мембрано-активных комплексонов ( МАК), поскольку именно среди них имеются ИСЭ с наиболее высокой селективностью. [12]
Для препаратов, используемых для внесения в почву, большое значение имеет их форма. Наиболее удобная - гранулированная в комбинации с удобрениями или на нейтральном носителе. [13]
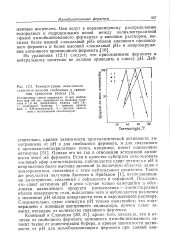 |
Температурные зависимости гидролиза казеина свободным и связанным трипсином ( быка. [14] |
Если в качестве субстрата использовать этиловый эфир ацетилтирозина, наблюдается сдвиг оптимума рН в направлении более высоких значений ( в щелочную область) даже с химотрипсином, связанным с этим нейтральным носителем. Такие же результаты получены Аксеном и Эрнбеком [1], исследовавшими химотрипсин, связанный с сефадексом и сефарозой. Показано, что сдвиг оптимума рН в этом случае только кажущийся и обусловлен накоплением продукта расщепления - ацетилтирозина вблизи поверхности геля, вследствие чего и наблюдаются различия в значениях рН вблизи поверхности геля и окружающего раствора. Следовательно, сдвиг оптимума рН только кажущийся; это подтверждено с помощью внутреннего индикатора, причем сдвиг зависит, очевидно, от количества связанного фермента. [15]
Страницы: 1 2