Sf-электрон
Cтраница 1
Большая подвижность Sf-электронов по сравнению с подвижностью 4 / - электронов обусловливает большую склонность актинидов к комплексообразованию и существование более высоких валентностей. [1]
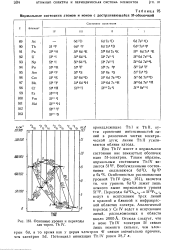 |
Нормальные состояния атомов и ионов с достраивающейся 51-оболочкой.| Основные уровни и переходы для тория, Th IV. [2] |
Ион ThIV имеет в нормальном состоянии вне замкнутых оболочек один Sf-электрон. Переходы 6d2D3 / 25 / J - 5f 2F5 / 2 r / t ведут к испусканию трех линий в красной и близкой к инфракрасной областях спектра. Аналогичный переход у Се IV ведет к испусканию линий, расположенных в области около 2000 А. [3]
Наличие сверхтонкой структуры фтора в спектре урана и отсутствие последней у неодима свидетельствует о том, что Sf-электроны участвуют в образовании заметной ковалентной связи. [4]
В ряду заурановых элементов орбиты 5 / стабилизируются дополнительно. В NpF6 имеется единственный Sf-электрон, в PuF6 - два спаренных 5 / - электрона, а в PuF4, PuF3, AmF3 и CmF3 - четыре, пять, шесть и семь Sf-элек-тронов соответственно. [5]
Актиноиды образуют аналогичные сульфидные фазы. Переходы f - d, характерные для лантаноидов, типичны и для актиноидов с той лишь разницей, что более высокое главное квантовое число Sf-электронов актиноидов вызывает большую энергетическую стабильность соответствующих f - конфигураций, а также образующихся в результате f - d - переходов / - конфигураций. Вследствие этого принципиальных различий в характере химических связей и в формировании физических и химических свойств в сульфидах различных элементов лантаноидов и актиноидов не наблюдается. Поэтому физические свойства сульфидов редкоземельных металлов приведены в гл. IV не применительно к каждому металлу, а даны в обобщенном виде. [6]
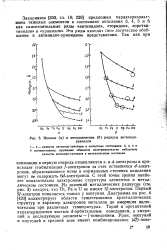 |
Ионные ( а и металлические ( б радиусы актинидо. [7] |
С этой точки зрения наиболее показательны электронные структуры элементов в металлическом состоянии. Из значений металлических радиусов ( см. рис. 3) следует, что Th, Ра и U не имеют 5 / - электронов. Первый Sf-электрон появляется только у нептуния. Диаграмма на рис. 4 [420] иллюстрирует области существования кристаллических структур и характер электронов металлов до америция включительно при различных температурах. Торий и протактиний характеризуются чистым rf - орбитальным поведением, а америций и последующие элементы - / - поведением. [8]
В главе VI уже указывалось, что актиниды рассматриваются как аналоги лантанидов. Современные работы по изучению спектров поглощения этих элементов подтверждают эту аналогию. Однако более низкие значения энергии связи Sf-электронов по сравнению с энергией связи 4 / - электронов обусловливают и определенные различия в свойствах лантанидов и актинидов, проявляющиеся, в частности, в появлении высших ( выше 4) валентных состояний и в большей их устойчивости. [9]
Нет сомнения, что существует вторая группа внутрирядных переходных элементов, в которых заполняется 5 / - подуровень, однако неясно, где действительно начинается этот ряд, где появляются 5 / - электроны. Трудность отнесения электрона к определенному подуровню атома для элементов, стоящих после актиния, заключается в близости величин энергии для 5f - и 6 -состояний. Энергии, выделяющейся при образовании химической связи, достаточно для перехода электрона с одного на другой энергетический уровень. Первый Sf-электрон должен был бы появиться у атома тория. Однако многие свойства этого элемента указывают на то, что его следовало бы поставить в подгруппу IV А под гафнием, а не в III А под церием. Протактиний и уран по их свойствам тоже больше подходят к подгруппам V А и VI А, нежели к празеодиму и неодиму. Однако сейчас есть обстоятельные спектроскопические и химические доказательства, подтверждающие мнение, что элементы, стоящие после актиния, образуют второй редкоземельный ряд и что Sf-электроны впервые появляются у протактиния. Несомненно, что у атомов этого ряда элементов, как и других переходных рядов, относительная энергия заполняемого уровня становится меньше по мере последовательного прибавления электронов. [10]
Нет сомнения, что существует вторая группа внутрирядных переходных элементов, в которых заполняется 5 / - подуровень, однако неясно, где действительно начинается этот ряд, где появляются 5 / - электроны. Трудность отнесения электрона к определенному подуровню атома для элементов, стоящих после актиния, заключается в близости величин энергии для 5f - и 6 -состояний. Энергии, выделяющейся при образовании химической связи, достаточно для перехода электрона с одного на другой энергетический уровень. Первый Sf-электрон должен был бы появиться у атома тория. Однако многие свойства этого элемента указывают на то, что его следовало бы поставить в подгруппу IV А под гафнием, а не в III А под церием. Протактиний и уран по их свойствам тоже больше подходят к подгруппам V А и VI А, нежели к празеодиму и неодиму. Однако сейчас есть обстоятельные спектроскопические и химические доказательства, подтверждающие мнение, что элементы, стоящие после актиния, образуют второй редкоземельный ряд и что Sf-электроны впервые появляются у протактиния. Несомненно, что у атомов этого ряда элементов, как и других переходных рядов, относительная энергия заполняемого уровня становится меньше по мере последовательного прибавления электронов. [11]
Страницы: 1