Обезвреживание - питьевая вода
Cтраница 1
Обезвреживание питьевой воды достигается обычно хлорированием, поэтому необходимо ограничивать содержание в ней фенолов. [1]
Впервые в крупном масштабе озон был применен в 1911 г. для обезвреживания питьевой воды на Петроградской фильтровальной станции производительностью по воде около 50 тыс. м3 / сутки. Позднее озон стали использовать на станциях для очистки питьевых вод во Франции и США. [2]
В особую группу химических методов следует выделить хлорирование и озонирование, наиболее часто применяемые для доочистки и обезвреживания питьевой воды на городских водопроводных станциях. [3]
Подобно некоторым другим окислителям ( таким, как хлор) озон обладает свойством обесцвечивать многие окрашенные органические вещества; благодаря этому он находит применение в качестве отбеливающего средства при обработке масел, воска, крахмала и муки. Озон обладает свойством убивать бактерии, и поэтому его применяют вместо хлора для обезвреживания питьевой воды. [4]
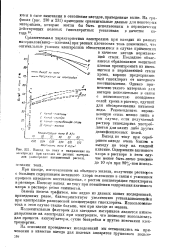 |
Выход по току и напряжение на электродах при катодах из разных материалов ( электролит насыщенный рассол. [5] |
Последнее объясняется образованием защитной пленки хромихромата из имеющегося в нержавеющей стали хрома, хорошо предохраняющей гипохлорит от катодного восстановления. Однако применение такого материала для катодов нежелательно в связи с возможностью попадания солей хрома в раствор, идущий для обезвреживания питьевой воды. Рекомендовать нержавеющую сталь можно лишь в том случае, если получаемый раствор гипохлорита употребляется для каких либо других дезинфекционных целей. [6]
По действующим в СССР санитарным правилам на всех питьевых водопроводах, питаемых водой из открытых источников, обязательно устройство приспособлений для дезинфекции ноды. Наиболее распространено добавление хлора в виде сгущенного ( жидкого) хлора или в виде хлорной извести; имеются еще способы дезинфекции ультрафиолетовыми лучами, озонированием и фильтрованием черев посеребренный песок. Доза хлора, требуемая для обезвреживания питьевой воды, зависит от содержания в ней органич. Продолжительность соприкосновения воды с, хлором дли обезвреживания воды достаточна ок. В СССР распространены 2 тина хлораторов: германский сист. Орнштенна и русский сист. Ремеениц-кого; последний представлен на фиг. [7]
Железные катоды, хотя и подвергаются разрушающему действию такой агрессивной среды, как пшохлорит, но соответственно подбирая толщину, можно обеспечить их работу в течение длительного срока. Сложнее обстоит дело с защитой гипохлорита от катодного восстановления, которое на железе достигает значительной величины. Добавление бихромата калия или хромирование катода в тех случаях, когда гигпохлорнт идет на обезвреживание питьевой воды, рекомендовать нельзя. [8]
Фенолы имеются во всех сточных водах, но особенно их много в сточных водах газостанций, работающих на торфе и бурых углях. Они состоят примерно из 50 % собственно фенолов ( C6HsCOOH), а в остальной части из их производных - крезо-лов, высших и двухатомных фенолов, например пирокатехина [ СбН4 ( ОН) 2 ] и др. Фенолы отлично растворяются в воде и особенно вредно действуют на животный и растительный мир водоемов и речных бассейнов. Содержание фенолов в воде в самой ничтожной концентрации ( 1: 100000000) при обычном способе обезвреживания питьевой воды ( хлорировании) придает воде неприятный привкус и запах хлорфенола, что делает воду непригодной для питья. [9]
Перманганат калия применяют в технике главным образом в качестве окислителя, в частности, для беления тканей, жиров, масел. Применение в медицине также основано на его сильных окислительных свойствах. Для этих же целей применяют и перманганат натрия, но в ограниченных количествах из-за трудности получения в чистом виде в сильной гигроскопичности. Са ( МпО4) 2 - 5Н2О применяют для обезвреживания питьевой воды. [10]
Перманганат калия, мировое производство которого составляет 30 - 40 тыс. т в год30, применяют главным образом в качестве окислителя, в частности, для беления тканей, жиров, масел. Применение в медицине также основано на его сильных окислительных свойствах. Для этих же целей применяют и перманганат натрия, но в ограниченных количествах из-за трудности получения в чистом виде и сильной гигроскопичности. Са ( МпО4) 2 - 5Н20 применяют для обезвреживания питьевой воды. [11]
Перманганат калия, мировое производство которого составляет 30 - 40 тыс. т в год30, применяют главным образом в качестве окислителя, в частности, для беления тканей, жиров, масел. Применение в медицине также основано на его сильных окислительных свойствах. Для этих же целей применяют и перманга-нат натрия, но в ограниченных количествах из-за трудности получения в чистом виде и сильной гигроскопичности. Са ( МпО2) 2 - 5Н2О применяют для обезвреживания питьевой воды. Согласно ГОСТ 5777 - 71, перманганат калия 1 -, 2 - и 3-го сортов должен содержать, соответственно, не менее 99 0, 98 0 и 95 0 % КМпО4 и не более: 0 3, 0 75 и 1 0 % двуокиси марганца, 0 05, 0 2 и 0 3 % сульфатов в пересчете на SO4 и 0 5, 0 5 и 2 0 % воды. Тарой для перман-ганата калия служат стальные барабаны и банки, которые запаиваются или завальцовываются. [12]
От количества растворенных солей зависит жесткость воды. Воду повышенной жесткости предварительно обрабатывают в специальных стационарных установках-водоумягчителях, где ее насыщают специальными химическими веществами-антинакипинами. Особые требования предъявляют к питьевой воде. В ней не должно быть болезнетворных бактерий, вызывающих заболевания желудочно-кишечного тракта человека, и вредных химических примесей. Для обезвреживания питьевой воды служат специальные устройства. [13]
Страницы: 1