Обезгаживание - образец
Cтраница 1
Обезгаживание образцов проводилось в течение 3 - 4 час. Газообразная NO при этом давлении в той же кювете не проявлялась в спектре. На Fe20s и СгаО3 проведена адсорбция NO при 150, однако никаких изменений в спектрах по сравнению с адсорбцией при 20 не наблюдалось. [1]
 |
Специальные плоские ампулы для образцов. а - пустил. б - с образцом. в - запаянная. [2] |
Для обезгаживания образцов используются нагреватели, форма которых в точности соответствует форме адсорбционных ампул. [3]
Эти данные относятся к иебольшой величине Q и получены при тщательном обезгаживании образцов перед каждым опытом. Ход температурных изменений показан стрелками. [4]
Простое обезгаживание образцов в эвакуированной стеклянной или кварцевой трубке при непрерывно возрастающей температуре с анализом выделяющихся газов может дать интересную информацию о их составе и примесях. Бартон и Говье ( 1965) приводят данные относительно ряда эластомеров и пластиков, представляющих промышленный интерес. Определение гелия, аргона и других редких газов в метеоритах и геологических объектах методом вакуумно-экстракционной масс-спектрометрии хорошо разработано в течение многих лет. Методика эксперимента относительно лроста. Навеску в несколько десятых миллиграмма вводят в молибденовый тигель, который затем помещают в охлаждаемый водой стеклянный сосуд. Газы идентифицируют, измеряют их количество и определяют изотопные отношения. [5]
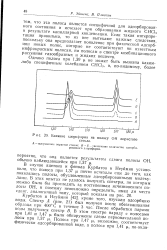 |
Влияние хлороформа на полосу ОН пористого. [6] |
Курбатов и Неуймин [42], кроме того, изучали адсорбцию воды. Спектр А ( рис. 21) был получен после обезгаживания образца при 400 С в течение 3 час. [7]
Эта температура отвечает температуре Таммана для перестройки поверхности. В работе [1] мы сообщали о том, что наблюдали некоторое спекание слоя платины при длительном обезгаживании образцов при 480, это также говорит о процессах перестройки частиц на поверхности силика-геля. Отсюда следует, что процессы кристаллизации в пределах одной частицы лла-тины при 500 не являются кинетически заторможенными. [8]
Совершенно очевидно, что применение реплик является весьма целесообразным при изучении препаратов, не стойких в обычных условиях электронно-микроскопического исследования. Они установили, что сравнительно хорошие реплики при температуре жидкого азота с сухих образцов могут быть получены после предварительного тщательного обезгаживания образцов. При исследованиях водных дисперсий охлаждение объекта следует производить медленно при одновременном осторожном эвакуировании. [9]
 |
Окисление СО. Поперечное сече-ние плоскости ( 001 кристаллической ре.| Окисление СО. Проекция пло-скости ( 011 кристаллической решетки за. [10] |
Закись меди является уникальным окислом, так как она имеет объемноцентрированную анионную решетку с катионами, расположенными по углам тетраэдра вокруг анионов. Половина отрицательных кислородных ионов выступает над геометрической плоскостью, в которой расположены ионы одновалентной меди, а другая половина утоплена под этой плоскостью. Стоун высказал предположение, что при температуре 200, при которой Винтер производил обезгаживание образца окисла, некоторая часть ионов кислорода переходит из утопленного положения в выступающее и, таким образом, располагается благоприятно для реакции обмена с атомами газовой фазы. Кроме того, едва ли между такими выступающими ионами кислорода и адсорбированным кислородом существует четкое различие. [11]
Удалить кислород полностью очень трудно; это легко продемонстрировать на растворе любого вещества с небольшими молекулами, как, например, бензол. Проделывайте над ним циклы замораживания-откачивания-размораживания и после каждого цикла проверяйте 7 ( быстрый метод определения Т, описан в гл. Обратите внимание, насколько долго нужно обезгаживать образец до получения постоянного Т1т Такой эксперимент, кроме того, позволит хорошо проверить ваше оборудование. Старайтесь проводить обезгаживание образца непосредственно перед измерением ЯЭО, поскольку кислород довольно быстро диффундирует внутрь образца даже в ампуле с краником. Очень полезно иметь вакуумную линию непосредственно в ЯМР-лаборатории. [12]
Совсем другими свойствами обладают частицы каталитически активных металлов с линейными размерами 8 - 50 А. В таком относительно узком интервале, отвечающем предельно дисперсным частицам, происходит быстрое изменение средних координационных чисел атомов на поверхности кристалла от значений, характерных для дефектов поверхности, вершин и ребер кристаллов, до значений, которые относятся к бесконечным граням кристаллов. Это позволяет изучить свойства активных центров при различии в ближнем порядке в поверхностном слое катализатора. Для такого изучения необходимо найти способ получения катализаторов, которые сочетают высокую дисперсность частиц с их устойчивостью при термообработке, необходимой для обезгаживания образцов. [13]
Термодесорбционные данные [75] показывают, что прочно связанная молекулярная вода в основном десорбируется при 520 К и что процесс завершается при 620 К, в то время как поверхностные гидроксильные группы удаляются при 640 К, а полное их удаление достигается при значительно более высокой температуре. Имеются данные, что образцы рутила, приготовленные гидролизом TiCU, содержат остаточный хлор, который облегчает удаление гидроксильных групп в процессе десорбции воды. Адсорбционно-десорбционное равновесие с молекулярной водой устанавливается быстро, но положение равновесия процессов гидроксилирование-дегидроксилирование менее определенно. Легкость регидроксилирования зависит от степени кристалличности образца. Слабо окристаллизованные образцы устойчивы к регидроксилированию даже при 670 К и давлении водяных паров 2 7 103 Па ( - 20 мм рт. ст.) [67], но для образцов с высокой степенью кристалличности регидроксилирование легко протекает уже при комнатной температуре. В целом полученные данные свидетельствуют, что для образцов с высокой степенью кристалличности равновесие гидроксилирование-регидроксилирование устанавливается достаточно быстро при комнатной температуре. Бренстедовская и льюисовская кислотность двуокиси титана исследована с использованием диагностических адсорбатов и ИК-спектроскопии. Образование поверхностного бикарбоната [77] при адсорбции двуокиси углерода указывает на присутствие некоторого количества основных гидроксильных групп. Однако их основность весьма слаба, так как обезгаживание образца при 300 К разрушает бикарбонат. Превращение поверхностных ионов кислорода в гидроксильные группы при диссоциативной адсорбции воды также говорит о бренстедовской основности поверхности. Считают [76], что эти функции связаны с присутствием двух типов гидроксильных групп. [14]
Страницы: 1