Область - фазовая диаграмма
Cтраница 1
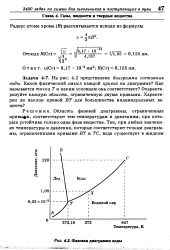 |
Фазовая диаграмма воды. [1] |
Области фазовой диаграммы, ограниченные кривыми, соответствуют тем температурам и давлениям, при которых устойчива только одна фаза вещества. [2]
В области фазовой диаграммы, соответствующей малым концентрациям В, кривые жидкой и твердой фаз можно приближенно считать прямыми. Обозначим через С концентрацию примеси В в твердой фазе, выпадающей в осадок из жидкой фазы, где концентрация примеси равна Ст. Отношение С / Ст k называется константой сегрегации. L, концентрация вещества В в котором равна С т, охлаждается с левого конца и затвердевает. [3]
Сказанное выше относится также к областям фазовой диаграммы с высокой концентрацией металла. Большое число металлов, например, такие, как титан, цирконий, тантал, торий и уран, растворяет значительное количество кислорода, что приводит к заметному изменению их термохимических свойств. Если относительная интегральная молярная свободная энергия металлической фазы уменьшается при добавлении кислорода настолько быстро, что это перекрывает тенденцию к увеличению летучести за счет наличия газообразной моноокиси, то в общей скорости эффузии наблюдается минимум. Возможно, что в системе торий - кислород также имеется минимум, но он расположен слишком, близко к чистому металлу и недостаточно глубок для того, чтобы его можно было обнаружить. [4]
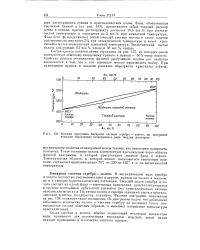 |
Фазовая диаграмма бинарной системы серебро - золото. на диаграмме-показано образование непрерывного ряда твердых растворов. [5] |
Такое состояние сплава соответствует прохождению через область фазовой диаграммы, в которой присутствуют жидкая фаза и а-фаза. [6]
Так или иначе, из-за наличия полиморфных модификаций области фазовой диаграммы между осью ординат и линией ОАВ на рис. 6.4 й и между осью ординат и линией 01 на рис. б б не являются, вообще говоря, однородными. Они в свою очередь разбиваются на участки, соответствующие различным кристаллическим модификациям. [7]
При построении многофазного уравнения состояния металла определяется свободная энергия вещества во всей практически интересной области фазовой диаграммы. Необходимо подчеркнуть, что, несмотря на довольно значительное число параметров в этих выражениях, большая их часть явно или неявно однозначно определяется по экспериментальным термодинамическим характеристикам металлов в различных участках фазовой диаграммы. Относительно небольшое число параметров уравнения состояния являются свободными, но их действие локализовано. Они имеют смысл характерных значений плотности и температуры перехода от одной области фазовой диаграммы к другой. [8]
Основной причиной, приводящей к нарушению термодинамической устойчивости любой химической модели в этой области фазовой диаграммы, как правило, является наличие больших отрицательных членов в выражениях для термодинамических функций и в уравнениях ионизационного и химического равновесия, связанных с кулоновскими корреляциями. [10]
Об зтой форме почти нет никаких данных, и неизвестно, в какой области фазовой диаграммы ее следует искать. [11]
Об этой форме почти нет никаких данных, и неизвестно, в какой области фазовой диаграммы ее следует искать. [12]
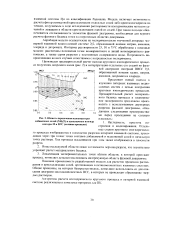 |
Область пересечения изоконцентрат. [13] |
Локализация экспериментальных точек вблизи области, в которой протекает процесс, позволяет детально исследовать интересующую область фазовой диаграммы. [14]
Страницы: 1 2 3 4