Область - кристаллизация
Cтраница 3
Изотермы такой диаграммы, ограничивающие области кристаллизации солей, аппроксимируются полиномами, что позволяет ввести эту диаграмму в память ЭВМ. При расчете МТБ производств второго класса, кроме общей информации о ХТС, необходимо знать химические реакции и их стехиометрические коэффициенты, степени превращения веществ, которые задаются проектировщиком. [31]
Указанные приемы применимы в равновесной области кристаллизации, если в исследуемом диапазоне относительных содержаний С0 равновесный коэффициент распределения от них практически, не зависит. Однако распространение таких способов оценки коэффициентов распределения на неравновесную область, как уже отмечалось в разд. [32]
Разумеется, для определения областей кристаллизации других фаз - А, В или С - необходимо совместить соответственно другие три тройные системы ( с общей им всем бинарной), которые отвечают другим граням пентатопа: ABC, DBC и ЕВС или DAB, ЕАВ и САБ. [33]
Это обусловило интенсификацию исследований в области кристаллизации, поскольку без знания условий образования кристаллов ( их чистоты, выхода), без надлежащего выбора растворителя невозможно реализовать процесс. [34]
Доминирующее положение в ней занимают области кристаллизации сульфата калия, шенита, эпсо-мита и сильвина. Из рисунка видно, что леонит появляется в присутствии хлорида магния уже при 25 С; при 55 С в этих условиях образуется лангбейнит. На изотерме появляется ряд гидратов сульфата магния, что обусловлено дегидратирующим действием хлорида магния. Эвтоническая точка системы характеризуется одновременной кристаллизацией карналлита, бишофи-та и кизерита. [35]
Этот максимум, расположенный в области кристаллизации а-твердого раствора, возможно связан с образованием соединения Zr30 с металлическим характером связи, аналогичного соединению Т130 в системе титан - кислород. Возможность образования соединения подобного состава требует дополнительного исследования точными методами физико-химического анализа. Аналогия диаграмм состояния этих двух систем с кислородом ограничивается областями [ 3 - иа-твердых растворов кислорода в титане и цирконии. [36]
Изложенные выше теоретические исследования в области кристаллизации твердых углеводородов имеют большое значение для регулирования процесса депарафинизации масел в смысле обеспечения надлежащего роста кристаллов, повышения скорости фильтрации и уменьшения содержания масел в гаче. Некоторые положения, основанные на этом материале, изложены ниже в разделе депарафинизации масел. [37]
Таким путем удается удовлетворительно разграничить области кристаллизации различных натриевых цеолитов в условиях наших опытов. [38]
На рис. 42 видны границы области кристаллизации гипса. Ее размеры весьма значительны. Вероятность выделения этой соли особенно велика из растворов, в которых много хлоридов. Преобладание ионов магния уменьшает ее незначительно, и только в присутствии избытка бикарбонатов для кристаллизации CaS04 - 2H20 требуется не менее 60 % SO в сумме анионов. Что же касается ионов кальция, то и в этом случае их достаточно в количествах 3 - 5 % в сумме катионов. [39]
Секторы на диаграммах составов аналогичны областям кристаллизации отдельных фаз в обычных диаграммах состояния. Чтобы более точно очертить границы между ними, а также постепенный ход изменений соотношения компонентов внутри каждого сектора, автор пользуется понятием энтропии, почерпнутым из теории информации. [40]
 |
Политермическая диаграмма границ полей.| Изотерма 0 С системы Sr ( OH2 - Н202 - Н20. [41] |
Область существования Са02 8Н30 ограничена областью кристаллизации льда. [42]
 |
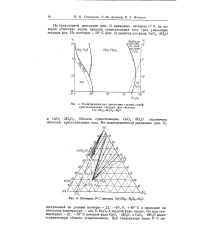
Изотермы растворимости в системах ( вес. %. КС1 - Ра06 - Н20 ( / и КС1 - СаО - Р205 - Н20 ( 77. [43] |
Причем наиболее заметно это в областях кристаллизации монокальцийфосфата при 20 - 40 и дикальцийфосфата при 60; при температуре 90 растворимость СаО в гипотетическом растворе увеличивается незначительно по сравнению с растворимостью в растворах чистой фосфорной кислоты. [44]
Лучи растворения пересекают треугольник NP75 - область кристаллизации двух солей. [45]
Страницы: 1 2 3 4