Область - низкий потенциал
Cтраница 1
Область низких потенциалов, при которых достигаются максимальные или близкие к ним заполнения поверхности продуктами хемосорбции. [1]
Области низких потенциалов ионизации во всех трех спектрах имеют более сложный вид. Они обусловлены ионизацией с разных валентных молекулярных орбиталей. Отнесения, приведенные на рисунке, отчасти основаны на расчетах, отчасти на учете того обстоятельства, что суммарные интенсивности полос приближенно пропорциональны числу электронов на ор-биталях, дающих вклад в эту полосу. Так, двукратно заполненная орбиталь должна давать полосу, в два раза более интенсивную, чем однократно заполненная. [2]
 |
Идеальная потенциостатическая анодная поляризационная кривая для нержавеющей стали в нейтральном хлоридном растворе. А В - выделение кислорода. АВ - коррозия. [3] |
Восстанавливающие кислоты или смеси кислот имеют тенденцию смещать катодные кривые в область более низких потенциалов, тем самым способствуя коррозии. Окислительные растворы смещают катодные кривые к более высоким потенциалам и благоприятствуют пассивности, если только катодные не оказываются в области таких высоких потенциалов, что пересекают анодную кривую на участке АВ. Это область перепассивации, где пленка становится неустойчивой из-за окисления. [4]
 |
Изменение параметров лампы при работе в режиме с малым потреблением. [5] |
Несколько необычные характеристики усилителя с малым потреблением мощности связаны с характером изменения параметров лампы в области очень низких потенциалов на аноде и экранной сетке. [6]
Природа адсорбционных центров и адсорбционных связей в области высоких анодных потенциалов существенно отличается от таковых в области низких потенциалов, поскольку важную роль в формировании этих центров, очевидно, играют оксиды платины. Разные формы хемосорбированного кислорода ведут себя различно по отношению к процессу хемосорбции органических веществ, показывая неодинаковые способности к вытеснению органическими частицами и окислительную активность. По-видимому, имеет место включение хемосор бированных органических частиц в окисную ленку. V 1OB является, например, близость адсорбируе-мости на окисленной платине третичных алифатических спиртов и их гомологов с неразветвленной цепью. Слабая адсорбируе-мость третичных ширтов в области низких потенциалов объясняется отсутствием в их молекуле наиболее легко отщепляемых атомов водорода у а - С-атома. [7]
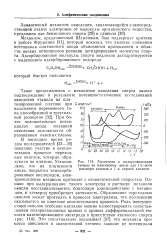 |
Емкостная и поляризационная кривые на платиновом аноде для 1 % - ного раствора этанола в 1 н. серной кислоте. [8] |
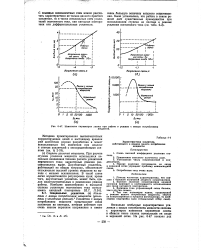
Механизм, предложенный Шлыгиным, был подвергнут критике в работе Фрумкина [31], который показал, что явление снижения потенциала платинового анода объясняется протеканием в области низких потенциалов реакции дегидрирования молекулы спирта. [9]
Скачок потенциала по окончании восстановления пятивалентного молибдена до трехвалентного состояния в среде 10 % - ной серной кислоты выражен менее отчетливр, чем первый скачок; он находится в области очень низких потенциалов, но вполне пригоден для использования в потенциометрическом титровании. [10]
Скачок потенциала по окончании восстановления пятивалентного молибдена до трехвалентного состояния в среде 10 % - ной серной кислоты выражен менее отчетливо, чем первый скачок; он находится в области очень низких потенциалов, но вполне пригоден для использования в потенциометрическом титровании. [11]
 |
Полярограмма катодного восстановления ионов. [12] |
Допустим, что в растворе имеется два вида катионов Mf и М, способных электролитически восстанавливаться при различных потенциалах. В области низких потенциалов на катоде происходит разряд более электроположительных катионов Mf. Участок вг полярограммы соответствует протеканию двух электродных процессов - разряду ионов Mf и М ( см. с. Таким образом, полярограмма имеет ступенчатый характер и состоит из вочн абв, игд. Потенциал, отвечающий значению тока, равному / д / 2, называется потенциалом полуволны ( Ф1 / 2) - Величина tpi / 2 не зависит от концентрации в растворе разряжающихся ионов, а определяется их природой и средой, в которой протекает электродная реакция. При качественном анализе раствора по экспериментально полученной полярограмме находят потенциалы полуволн и сравнивают их с уже известными значениями tpj 2 для различных ионов. [13]
Побочные процессы не рассматриваются, хотя при высоких плотностях тока растворение металлов и пленок будет сопровождаться одновременным выделением кислорода и фактические плотности тока будут более высокими. В области низких потенциалов наряду с растворением металла может происходить выделение водорода. [14]
Это прямое следствие фундаментального свойства интерференционной плотности PJ -: накопление электронного заряда в области связи. При этом электронный заряд перемещается из областей низкого потенциала, вблизи ядер, в область менее отрицательного потенциала, вблизи центра связи. Ясно, что такое перемещение заряда увеличивает потенциальную энергию. Попытки оценить увеличение потенциальной энергии за счет перераспределения электронной плотности часто приводили к ошибочным заключениям. [15]
Страницы: 1 2