Облегчение - восстановление
Cтраница 2
 |
Схема блокировки защиты. [16] |
Длительные качания и асинхронный ход допускаются в течение не более 3 мин. За это время персонал должен принять меры для облегчения восстановления синхронизма. Если эти меры оказались неэффективными, должно быть произведено разделение систем. Возможность возникновения длительного асинхронного хода является недостатком такого способа АПВ. [17]
Как уже указывалось выше, на активной поверхности металлов скорость восстановления ионов металла значительно выше, чем на пассивной. Действительно, с увеличением концентрации сульфата аммония наблюдается резкое облегчение восстановления ионов марганца, что видно по увеличению доли тока, идущего на восстановление ионов марганца ( см. рис. 5, стр. [18]
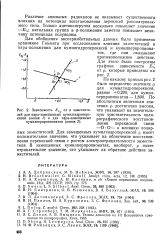 |
Зависимость., от а заместителей для пара-замещенных кумилгидроперекисей ( линия / и для пара-замещенных кумилперпропионатов ( линия 2. [19] |
Для замещенных кумилгидроперекисей р имеет положительное значение, что указывает на облегчение восстановления перекисной связи с ростом электроотрицательности заместителя. В замещенных кумилперпропионатах, наоборот, р имеет отрицательное значение, что указывает на обратное действие заместителей. [20]
Поскольку наиболее часто одним из реагентов при электрохимическом восстановлении является ион водорода, следующая часть этого раздела будет посвящена рассмотрению роли протонов в облегчении восстановления. [21]
Влажные сульфиды сурьмы растворяются при нагревании с серной кислотой и сульфатом калия или сульфатом аммония. Для определения сурьмы и других элементов, образующих летучие хлориды, поступают следующим образом. Переносят 1 г тонко измельченной пробы в колбу Кьельдаля, прибавляют 5 г сульфата аммония, 1 г сульфата калия, 15 мл серной кислоты и около 0 2 г серного цвета для облегчения восстановления сурьмы и мышьяка до трехвалентного состояния. Смесь нагревают на голом пламени сначала осторожно, потом более сильно, пока не исчезнет свободная сера и раствор не станет бесцветным. Колбу охлаждают, давая плаву растекаться по стенкам сосуда, и прибавляют 25 мл воды и 2 - 3 г винной кислоты. Нагревают до полного растворения растворимых солей, фильтруют, если это необходимо, умеренно промывают остаток разбавленной ( 1: 9) серной кислотой и затем водой для удаления кислоты. [22]
Во всех работах показана неравноценность а - и - положений в молекуле антрахинона. По нашему мнению, различия в поведении а - и - заместителей в первую очередь объясняются тем, что при нахождении заместителей в а-положении значительную роль играют стерические эффекты. Указанные эффекты приводят к тому, что галоидный атом, находящийся в а-положении -, теряет в зависимости от его размера в большей или меньшей мере способность к сопряжению с карбонильной группой и, следовательно, приобретает в определенной степени свойства галоидного заместителя в алифатических соединениях. Такие эффекты в полярографии проявляются в облегчении восстановления молекул по галоиду. [23]
Многие органические вещества дают аномальные предволны, которые наблюдаются при высоких концентрациях при потенциалах менее отрицательных, чем основная волна. Сумма этих двух волн пропорциональна концентрации в соответствии с уравнением Ильковича I уравнение ( 7) 1, справедливым для волн, контролируемых диффузией. Однако высота первой волны пропорциональна концентрации только при низких концентрациях; при увеличении концентрации высота предволны стремится кпредельномузначению. Возникновение этой предволны чаще всего связано с облегчением восстановления в адсорбированном слое. При низких концентрациях поверхность ртутной капли заполнена не нацело, поэтому повышение концентрации может приводить к увеличению адсорбционного тока. Если же поверхность заполнена, повышение концентрации не может привести к увеличению адсорбционного тока, и только высота нормальной волны продолжает возрастать. [24]
Развивая концепцию иерархической оптимизации в аспекте режимно-технологических расчетов, А.И. Гарляускас выделяет два подхода к решению задачи оптимизации режима газопровода: первый сводится к единому процессу оптимизации распределения давлений по трассе и режимов КС, второй, который автор считает более выгодным, предусматривает декомпозицию с выделением КС в качестве подсистемы. Такой подход укладывается в схему иерархической оптимизации, причем в качестве внешних параметров фигурируют давления на входе и выходе КС и расход через нее. Задача построения ОДР не рассматривается, АОХ КС представлены в графическом виде как функции критерия ( мощность, топливный газ) в зависимости от расхода, давления выступают как параметры. Для решения координирующей оптимизационной задачи ( третий этап) предлагается процедура динамического программирования. Для облегчения восстановления оптимальных управляющих воздействий на КС ( четвертый этап) указано, что можно использовать построенные заранее зависимости управлений от внешних параметров. Приводятся примеры модельного характера. [25]
Во всех работах показана неравноценность а - и [ З - положений в молекуле антрахинона. По нашему мнению, различия в поведении а - и ( 3-заместителей в первую очередь объясняются тем, что при нахождении заместителей в u - положении значительную роль играют стерические эффекты. Эти эффекты могут быть настолько велики, что молекула даже перестает быть копланарной и поэтому а-заме-стители оказывают меньшее влияние на значение Ei / 2 карбонильных групп в молекуле антрахинона, чем те же заместители, находящиеся в ( 5-положении. Указанные эффекты приводят к тому, что галоидный атом, находящийся в а-положении, теряет в зависимости от его размера в большей или меньшей мере способность к сопряжению с карбонильной группой и, следовательно, приобретает в определенной степени свойства галоидного заместителя в алифатических соединениях. Такие эффекты в полярографии проявляются в облегчении восстановления молекул по галоиду. [26]
В предыдущем разделе мы видели, что фосфорилирование делает возможным окисление карбонильных групп в карбоксильные без рассеяния энергии и может иметь то же значение и на других стадиях перехода водорода от Сахаров к кислороду. Сейчас мы увидим, что фосфорилирование может также привлекаться для объяснения восстановления двуокиси углерода в фотосинтезе. Рубен [36] считал, что карбоксильная группа в ком - ллексе С02 может фосфоршшроватъся для облегчения восстановления. [27]
Результаты исследования каталитического выделения водорода под действием белков и некоторых других серусодержащих соединений в присутствии солей кобальта показали, что каталитическая активность обусловлена сульфгидрильными группами, водород которых под влиянием солей кобальта разряжается на электроде со значительным снижением перенапряжения. Одним из необходимых условий возникновения каталитической волны следует считать образование комплекса вещества, содержащего сульфгидрильные группы, с ионами кобальта. Для объяснения того, что каталитическая волна появляется при потенциалах, при которых кобальт уже должен быть полностью выделен на электроде, можно было бы предположить, что координационная связь лиганда, вероятнее всего SH-группы, сохраняется и после выделения кобальта. Бржезина [60] с помощью стационарного капельного электрода показал, что выделенный на электроде атомарный кобальт не вызывает каталитическую активность. Влчек [61] тем не менее доказал возможность существования нульвалентных комплексов; для данного случая связь SH-групп с атомами кобальта на поверхности электрода может, по-видимому, способствовать облегчению восстановления водорода. Протоны, отбираемые от SH-группы в результате электрохимической реакции, заменяются новыми при их последующей реакции с донорами протонов, находящимися в растворе, например - S - NH - SH NHj, вследствие чего возникает каталитический ток. [28]
Результаты исследования каталитического выделения водорода под действием белков и некоторых других серусодержащих соединений в присутствии солей кобальта показали, что каталитическая активность обусловлена сульфгидрильными группами, водород которых под влиянием солей кобальта разряжается на электроде со значительным снижением перенапряжения. Одним из необходимых условий возникновения каталитической волны следует считать образование комплекса вещества, содержащего сульфгидрильные группы, с ионами кобальта. Для объяснения того, что каталитическая волна появляется при потенциалах, при которых кобальт уже должен быть полностью выделен на электроде, можно было бы предположить, что координационная связь лиганда, вероятнее всего SH-группы, сохраняется и после выделения кобальта. Бржезина [60] с помощью стационарного капельного электрода показал, что выделенный на электроде атомарный кобальт не вызывает каталитическую активность. Влчек [61] тем не менее доказал возможность существования нульвалентных комплексов; для данного случая связь SH-групп с атомами кобальта на поверх ности электрода может, по-видимому, способствовать облегчению восстановления водорода. Протоны, отбираемые от SH-группы в результате электрохимической реакции, заменяются новыми при их последующей реакции с донорами протонов, находящимися в растворе, например - S - NHJ - SH NH3, вследствие чего возникает каталитический ток. [29]
Брдичка показал [67-69], что если один из компонентов обратимой редокс-системы адсорбируется на ртутном электроде значительно сильнее другого, то на полярограммах наряду с обычной диффузионной волной возникает еще так называемая адсорбционная волна, которая по свойствам резко отличается от диффузионной. Рассмотрим это явление подробнее для катодных процессов, когда продукт реакции адсорбируется лучше деполяризатора. При малых концентрациях деполяризатора на полярограмме наблюдается лишь одна волна, высота которой растет пропорционально концентрации. Однако при увеличении концентрации высота волны достигает некоторого постоянного значения и далее уже не зависит от концентрации деполяризатора. По достижении этой волной предела при более отрицательных потенциалах появляется и растет вторая волна, причем суммарная высота обеих волн увеличивается пропорционально концентрации деполяризатора и соответствует диффузионному току данного деполяризатора. По мнению Брдички, облегчение восстановления деполяризатора обусловлено выигрышем энергии при адсорбции продукта его восстановления. [30]
Страницы: 1 2