Атомный обмен
Cтраница 1
Атомный обмен происходит без выворачивания тетраэдра по цепной схеме, приведенной на стр. Ясно, что скорость этого процесса зависит от прочности связи С - X. По кинетическим данным, энергия этой связи в RGH2J равна 50 кал. Энергии связей С - Вг в молекулах СН3Вг, СН3Вг2, СНВг3 и СВг4 равны соответственно 67 5; 62 5; 55 5 и 49 кал. [1]
Предполагают, что при атомном обмене происходит смыкание участников реакции с образованием промежуточного соединения. [2]
Ясно поэтому, что скорость атомного обмена должна возрастать при накоплении атомов галоида в молекуле, при переходе от нормальных радикалов к радикалам изостроения и при замене водорода в СН3Х метильными радикалами. [3]
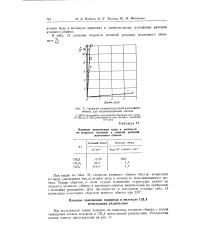 |
Скорости атомных реакций изотопного обмена для иодозамещенных метана. [4] |
Как видно из табл. И, скорость атомного обмена быстро возрастает по море увеличения числа атомов иода в молекуле иодозамещенного метана. Таким образом, в этом случае изменение структуры влияет па скорость атомного обмена в противоположном направлении по сравнению с ионными реакциями. [5]
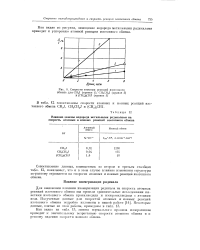 |
Скорости атомных реакций изотопного. [6] |
Как видно из табл. 13, замена нормального пропила изопропилом приводит к значительному возрастанию скорости атомного обмена и к резкому падению скорости ионного обмена. [7]
Другое свидетельство в пользу радикального механизма можно получить, сопоставляя потенциалы полуволн галоидалкилов со скоростями атомного обмена галоидалкилов с галоидами. [8]
При этом условии величина изотопного обмена приблизительно пропорциональна продолжительности освещения, как это следует из приведенной выше формулы для скорости атомного обмена. [9]
Как видно из табл. И, скорость атомного обмена быстро возрастает по море увеличения числа атомов иода в молекуле иодозамещенного метана. Таким образом, в этом случае изменение структуры влияет па скорость атомного обмена в противоположном направлении по сравнению с ионными реакциями. [10]
Присутствуя в твердом растворе, W и Мо повышают его термическую стойкость путем торможения процессов разупрочнения при высоких температурах. Они увеличивают температуру рекристаллизации твердого раствора, тормозят процессы диффузии, без которых не может происходить атомный обмен при коагуляции и рекристаллизации. [11]
Специфическая особенность реакций обмена одинаковыми атомами состоит в том, что молярные концентрации реагирующих компонентов остаются неизменными. Поэтому для таких реакций константы в уравнениях ( 5) и ( 6), а также сама скорость обмена ( г) одинаковыми атомами должны оставаться постоянными. При данных концентрациях компонентов скорость атомного обмена должна зависеть только от строения реагирующих веществ, среды и температуры. Однако обнаружить обмен одинаковыми атомами ( допустим Х), а тем более измерить его скорость без введения меченых атомов, принципиально невозможно, поскольку атомы данного изотопа неразличимы. Введение же атомов другого изотопа X с целью наблюдения за скоростью атомного обмена существенно усложняет картину. Во-первых, следует иметь в виду, что количество меченых атомов X составляет только часть всех атомов X, и их концентрация непрерывно меняется в каждом из компонентов в процессе обмена; во-вторых, при оценке скорости атомного обмена необходимо принимать во внимание зависимость скорости перехода меченого атома от степени симметрии реагирующих молекул, а также учитывать обратный обмен и, наконец, в-третьих, нужно вносить соответствующую поправку на изотопный эффект. По мере изменения величин х т у скорости перехода атомовХ будут изменяться и достигнут постоянного значения при равновесии. [12]
При дальнейшем нагревании некоторая часть поглощенной энергии расходуется атомами в процессе изменения местоположения частиц и нарушения упорядоченности системы. При любой температуре должно поддерживаться динамическое равновесие, и только часть атомов оказывается способной к перемещению. В последнем случае некоторая часть поглощенной энергии расходуется на увеличение внутренней энергии молекул, а другая - на увеличение степени диссоциации. Температура Тс, возможно, достигается тогда, когда атомный обмен в кристаллическом сплаве совершается легко, потому что средняя необходимая для этого энергия равна значению 2kTc, соответствующему равномерному распределению. После того как упорядоченность системы будет полностью нарушена, уже не потребуется на это затрачивать энергию и теплоемкость, естественно, уменьшится. При Тс исчезают все признаки упорядоченности и распределение атомов обоих типов становится случайным. [13]
Поскольку третьи частицы не участвуют в химической реакции, их концентрация остается постоянной. Таким образом, в действительности идет реакция третьего порядка. Для типичных реакций второго порядка ( например, перечисленных в табл. 2) присутствие третьей частицы не является необходимым; например, атомный обмен в реакциях типаЛ2 52 - 2АВ очевидно, может происходить при двойных столкновениях. Если, однако, химическое превращение относится к типу Az - 2BC - 2ABC, то необходимо, чтобы в одно и то же время три молекулы встретились в одном месте, если только реакция не протекает через ряд последовательных стадий. [14]
Каталитически активные поверхности никеля и вольфрама2 даже при температуре жидкого воздуха вызывают обмен орто - и пара-молекул водорода ( стр. Первая реакция может быть обусловлена локальными магнитными полями. Атомный же обмен обязательно требует разрыва ко-валентной связи. При этом существенно, что атомный обмен требует примерно одинаковой энергии активации, независимо от того, идет ли он как реакция на поверхности при низких температурах или как высокотемпературная газовая реакция со свободными атомами ( стр. [15]
Страницы: 1 2