Анализ - равновесие
Cтраница 1
Анализ равновесия природный газ - переохлажденная вода весьма существен при определении точки росы газа по влаге с использованием влагомеров конденсационного типа ( что отмечалось в гл. [1]
Анализ равновесия в системе U-O-C проводился с помощью программы Астра и с помощью разработанного в РНЦ Курчатовский институт программного комплекса Химический Верстак, который представляет собой специализированную компьютерную программу для моделирования, проектирования и оптимизации широкого спектра процессов, реакторов и технологий. Комплекс Химический Верстак включает в себя широкий набор моделей технологических процессов, исчерпывающие базы данных и использует достоверные и проверенные методы решений. [2]
Анализ равновесия в системе U-0 - C проводился с помощью программы Астра и с помощью разработанного в РНЦ Курчатовский институт программного комплекса Химический Верстак, который представляет собой специализированную компьютерную программу для моделирования, проектирования и оптимизации широкого спектра процессов, реакторов и технологий. Комплекс Химический Верстак включает в себя широкий набор моделей технологических процессов, исчерпывающие базы данных и использует достоверные и проверенные методы решений. [3]
Анализ равновесий производится термодинамическими методами, а для объяснения наблюдаемых закономерностей используется теория растворов. Подобный подход особенно необходим, так как в связи со все более расширяющимся практическим использованием экстракции для разделения ядерных материалов [1], редкоземельных элементов [2] и цветных металлов [3] по экстракции публикуется очень много работ, а интерпретация результатов часто ограничивается элементарными химическими расчетами на основании закона действующих масс, в которых вместо активностей используются концентрации. [4]
Анализ равновесия изолированной системы имеет большое практическое значение, ибо в качестве изолированной всегда можно рассматривать составную систему, образованную любой изучаемой системой и окружающей средой. Однако на практике часто встречаются и неизолированные системы; примером здесь может служить двухфазная система, находящаяся в условиях постоянных давления и температуры. [5]
 |
Направления преимущественной поверхностной диффузии на грани куба. [6] |
Анализ равновесия физической адсорбции ( проведен в главе 12.4) можно применить и к хемосорбции. При хемосорбции речь идет об образовании поверхностного соединения ( поверхностной фазы) между частицами адсорбата и адсорбента. В противоположность физической адсорбции для образования соединения на поверхности необходима энергия активации, из-за чего процесс химической адсорбции затруднен. Энергетический барьер, однако, может быть настолько мал, что уже при комнатной температуре может протекать хемосорбция. [7]
Преимущество анализа равновесия, т.е. сравнительной статики, в том, что в расчет принимаются все последствия любых экзогенных изменений, таких как сокращение предельных издержек какой-либо фирмой. [8]
При анализе равновесий ( 4) - ( 6) следует иметь в виду, что радикал II и молекула V образуют внутримолекулярную водородную связь. [9]
 |
Экспериментальные данные для реакции FlAKNa - ПДМАЭМ, представленные в координатах уравнения. [10] |
Описанный выше анализ равновесий кооперативных реакций между слабыми полиэлектролитами не основывается на конкретной модели процесса, что позволяет в самой общей форме анализировать данные эксперимента. [11]
В основе анализа равновесия лежит правило фаз - оно для к-компонентных и ф-фазных систем позволяет установить число степеней свободы р, иначе - интенсивных свойств ( фактически - управляющих воздействий), которые могут быть выбраны произвольно, т.е. навязаны системе извне. [12]
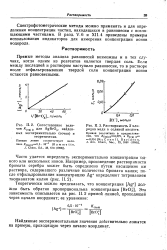 |
Сопоставление величин К ( тв о для AgBrO3, найденных экспериментально ( точки и теоретически. [13] |
Прямые методы анализа равновесий возможны и в тех случаях, когда одним из реагентов является твердая соль. Если между последней и раствором наступило равновесие, то в растворе после отфильтровывания твердой соли концентрации ионов остаются равновесными. [14]
В результате анализа равновесия 2О - О О2 - авторы [24] выявляют, какие наиболее вероятные типы комплексов SiAOy присутствуют в расплаве в зависимости от температуры и природы катиона Me. Аналогичный, но более строгий подход к оценке типов комплексных анионов развит Ван-Везером [25] для фосфатов. Он рассматривает равновесия между четырьмя структурными единицами при различных температурах и составах. [15]
Страницы: 1 2 3 4