Образец - кислота
Cтраница 2
СЖК С7 - С9, С10 - Cje и С17 - С20, проводят с учетом содержания как основной, так и сопутствующих кислот в индивидуальных образцах кислот. [16]
С), часто дает важные данные для установления строения исходных веществ. Необходимый для сравнения образец меллофановой кислоты может быть легко получен окислением мезитиленкарбоновой кислоты ( приготовленной из броммезитилена) азотной кислотой при 170 - 180 С. [17]
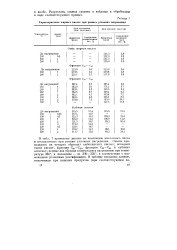 |
Характеристика жирных ислот при разных условиях нагревания. [18] |
В табл. 7 приведены данные по изменению кислотного числа и неомыляемых при разных условиях нагревания. Опыты проводились на четырех образцах шебекинских кислот: исходной смеси кислот, фракции С510 - С21, фракции С17 - С21 и кубовых остатках; первые два образца подвергались нагреванию при температуре 260, а последние - до 300 - 320, в соответствии с возможными условиями ректификации. [19]
Однако наличие максимума полосы люминесценции водного раствора полипропионовой кислоты в видимой области указывает на то, что в растворе существу ют, до вольно длинные блоки эффективного сопряжения, а значит, и жесткие участки полиэлектролита. Равенство длин этих участков для образцов полипропиоловой кислоты, полученных радиационной жидкофазной и твердофазной полимеризацией ( положение максимумов полос люминесценции растворов совпадает), позволяет более четко выявить влияние конфигурации основной цепи полипроетиолавой кислоты на степень ее диссоциации. [20]
Надежность определения энергий сгорания соединений, содержащих хлор, была подтверждена путем измерения величины Af / c вторичного стандарта - пара-хлорбензойной кислоты. Для этих измерений были использованы 2 образца кислоты, тщательно очищенные и проанализированные во Всесоюзном научно-исследовательском институте метрологии, чистотой 99 97 и 99 98 мол. [21]
Иллюстрацией может служить рис. 53, на котором изображена зависимость оптического вращения раствора поли - Ь - глутаминовой кислоты ( 0 5 % - ный раствор, рН 7) от длины волны. Вращение измеряли, помещая в прибор ячейку с образцом полиглутами-новой кислоты и ячейку с - крезолом; обе ячейки располагались последовательно одна за другой. Концентрацию - крезола подбирали так, чтобы получить суммарное поглощение А, обусловленное хромофором n - крезола и фоном полипептида при длине волны 276 м и, указанное на каждой приведенной на рисунке кривой. Поскольку оптически неактивный - крезол отделен от полипептида, наблюдаемое аномальное поведение исследуемой системы следует объяснить наличием артефактов. Артефакты обусловлены главным образом уменьшением интенсивности света при выбранной длине волны и прохождением паразитного света, который вызывает ненормальное оптическое вращение. Таким образом, чем выше поглощение, будь оно обусловлено растворителем или раствором, тем ярче выражены артефакты. [22]
После обработки щелочью описанным вине способом в исходной кислоте наряду с цис-изоыером образовался изомер, соответствующий транс-форме кислоты ( ряс. В табл. 2 представлены результаты хроматографического анализа до и после изомеризации трех образцов диизопропилкротоновой кислоты с различным исходным содержанием транс-изомера. [24]
Повышение электропроводности с ростом содержания остатков катализаторов или других примесей, а также при пластификации полимеров может быть связано как с возрастанием подвижности уже имеющихся в полимере носителей, так и с увеличением числа носителей [ 6, с. Поверхностная электропроводность полиметилмета-крилата, полистирола и полиизобутилена значительно повышается при нанесении на поверхность образцов кислот и щелочей и с увеличением давления паров воды. Адсорбированные на поверхности полимера молекулы ионогена способны диссоциировать и проводить ток лишь при наличии пленки воды толщиной порядка размера молекулы. [25]
Затем раствор охлаждают, выпавший осадок отсасывают и сушат. Депрессии температуры плавления с образцом я-кумаровой кислоты не обнаружено. Таким образом, основным продуктом реакции ( выход 36 5 % от теории) является диаммониевая соль 4-окси-бензшшдвнмалоновой кислоты. Из маточного раствора после отделения последней через двое суток выпадает 1 8 г азотсодержащего вещества, растворимого в кислотах и щелочах. При дальнейших перекристаллизациях температура плавления не изменяется. [26]
Решение этой задачи классическим методом заключается в том, что вначале определяют содержание отдельных компонентов по известным методикам ( HN03 - титрованием щелочью, a N02 - це-риметрически) и количество воды находят по разности. Согласно авторам [162] влажность белой дымящей азотной кислоты можно определить по Фишеру следующим образом. Образец кислоты осторожно нейтрализуют избытком смеси ( примерно 10 см3) пиридин - диметилформамид и далее прибавляют известное количество реактива Фишера, превышающее содержание воды. Избыток реактива обратно титруют стандартным раствором воды в метаноле с биамперометри-ческой индикацией конечной точки. Как видно из данных, приведенных в табл. 1.8, двуокись азота вплоть до концентрации 1 5 % не мешает титрованию воды по описанному способу. [27]
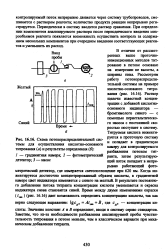 |
Схема потокораспределительной системы для осуществления кислотно-основного титрования ( а и результаты определения ( б. [28] |
В отличие от рассмотренных выше проточно-инжекционных методов титрование в потоке основано на измерении не высоты, а ширины пика. Раствор щелочи известной концентрации с добавкой кислотно-основного индикатора - бромтимолого синего - с помощью перистальтического насоса с постоянной скоростью поступает в систему. Титруемая кислота инжектируется в проточную систему и попадает в градиентную камеру для контролируемого разбавления потоком таг-ранта, затем результирующий поток попадает в непрерывно работающий фотометрический детектор, где измеряется светопоглощение при 620 нм. Когда инжектируется достаточно концентрированный образец кислоты, в градиентной камере цвет индикатора изменяется с синего на желтый. В результате постоянного добавления потока титранга концентрация кислоты уменьшается и окраска индикатора снова становится синей. [29]
Известно, что существенным недостатком китового жира, тормозящим применение его в мыловарении, является наличие характерного рыбного запаха. Однако во всех образцах кислот, перешедших в осадок с карбамидом, этот запах совершенно отсутствовал, что свидетельствует о целесообразности применения карбамидного метода при использовании китового жира. [30]
Страницы: 1 2 3