Образец - окись - цинк
Cтраница 2
Фуйита и Кван [112] обнаружили фотоадсорбцию кислорода при 18 для образца окиси цинка, предварительно прогретого в течение часа при 300 в кислороде ( р 10 мм) и затем охлажденного перед откачкой. Теренин и Солоницын [113] также наблюдали это явление на окисленной окиси цинка, но они не сообщают подробностей. Возможность фотоадсорбции за счет возбуждения газообразного кислорода можно исключить, потому что в близкой ультрафиолетовой области этот газ не поглощается. [16]
Согласно наблюдениям этих авторов, облучение не оказывает влияния на каталитическую активность некоторых образцов окиси цинка, содержащих большой избыток междоузельных атомов цинка. Они объясняют этот факт, экспериментально подтвержденный также Берри и Робертсом [20], наличием конкуренции между молекулами СО и междоузельными атомами цинка при захвате дырок. [17]
Парравано, Фридрик и Будар [19] сообщили, что при адсорбции водорода на ряде образцов окиси цинка изотопный эффект не наблюдается. Это означает, что изотопный эффект связан с взаимодействием между газообразным водородом и адсорбированным слоем. [18]
Наиболее убедительным доказательством того, что эти реакции обусловлены подвижными электронами, является поведение образцов люминесцентной окиси цинка. Такие захваченные ловушкой электроны, хотя и находятся в состояниях с повышенной энергией, расположенных только немного ниже зоны проводимости, закреплены неподвижно на локализованных участках. Они не способны мигрировать к поверхности и хемосорбировать кислород или перекись водорода. Достаточно характерным является то, что такая активация для люминесценции влечет за собой дезактивацию в отношении катализа: реакции образования и разложения перекиси водорода на этих препаратах ZnO замедляются. Ниже приведены некоторые новые примеры. [19]
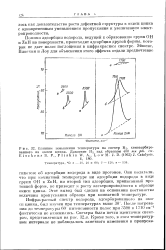 |
Влияние повышения температуры на спектр Н2, хемосорбиро-ванного на окиси цинка. Давление Н2 над образцом 400 мм рт. ст. Е i s с h e n s R. Р., Р 1 i s k i 11, Low M. J. D. ( 1962 J. Catalysis. [20] |
Они полагали, что при комнатной температуре ни адсорбция водорода в виде групп ОН и ZnH, ни второй тип адсорбции, приписанный протонной форме, не приводит к росту электропроводности с образце окиси цинка. Этот вывод был сделан на основании постоянства величины пропускания образца при комнатной температуре. [21]
Испытывались также образцы окиси цинка, изготовленные в другом режиме, и образцы химически чистой окиси цинка, но они обладали меньшей яркостью люминесценции и в дальнейшем не применялись. [22]
 |
Скорости обмена водорода с дейтерием. [23] |
Эти данные заставляют нас предположить, что контролирующей стадией в данном случае служит переход электронов ионам Н и D при десорбции. При водородной обработке образцов окиси цинка, содержащих хемосорбированный кислород, поверхность катализатора быстро освобождается от него. [24]
На поверхности окиси цинка осуществляются два типа адсорбции водорода. Одна форма адсорбции имеет место при температуре ниже 100, при этом не происходит изменений в электропроводности образца окиси цинка. При более высоких температурах наблюдается увеличение количества адсорбированного водорода, и в течение этого процесса электропроводность образца заметно растет. [25]
Дифференциальный фотоэлектрический фотометр, служивший для измерения интенсивности люминесценции, состоял из двух сурьмяно-цезиевых вакуумных фотоэлементов СЦВ-3, включенных навстречу друг другу. Зеленовато-желтый свет люминесценции от образца окиси цинка фокусировался стеклянной линзой на один фотоэлемент, на другой фокусировался свет люминесценции эталона. [26]
Прошло уже 50 лет с тех пор, как Айбнер [106] впервые сообщил о фотоактивности окиси цинка. За это время было опубликовано много сведений, но мы будем ссылаться здесь только на последние работы, имеющие отношение к основной теме данной статьи. В 1954 г. Мясников и Пшежецкий [107] провели простой, но очень изящный эксперимент, в котором два образца окиси цинка были помещены рядом в одном откачанном сосуде. Один образец облучали ультрафиолетовым светом, и его проводимость при этом возрастала; однако одновременно наблюдалось падение проводимости у другого образца, который был защищен от облучения. [27]
 |
Определение микрофазы Ag2O или окиси церия в ZnO. [28] |
Метод определения микрофазы серебра и суммарного содержания серебра в окиси цинка, легированной серебром, основан на извлечении микрофазы растворимых солей и окиси серебра путем селективного растворения при обработке образца горячей водой. Время проведения анализа - 1 час. В табл. 1 представлены результаты определения серебра в образцах окиси цинка, легированных серебром. [29]
На первый взгляд высокая каталитическая активность окиси цинка в реакциях, включающих в качестве стадии диссоциативную хемосорбцию водорода, кажется удивительной. В самом деле, окись цинка представляет собой диамагнетик, и d - зоны, связанные с ионами Zn2, заполнены. В настоящее время твердо установлено [18], что для низкотемпературной хемосорбции водорода существенное значение имеют незаполненные rf - зоны переходных металлов. Недавно Кемболл [19] отметил, что пленки металлического цинка совершенно не катализируют реакцию обмена между NH3 и D2 - в соответствии с заполненностью d - зоны металлического цинка. С другой стороны, образец окиси цинка до активации также неактивен по отношению к хемосорбции водорода. Однако если пленку металлического цинка после приготовления специально загрязнить кислородом, то, согласно Кемболлу, она становится гидрогенизационным катализатором. Наоборот, окись цинка активируется после предварительной обработки в вакууме или в атмосфере водорода. Это наводит на мысль, что активная система представляет собой нечто среднее между цинком и окисью цинка, возможно - нестехиометрическую окись цинка. [30]
Страницы: 1 2