Образование - аммиакат
Cтраница 1
Образование аммиакатов возможно и при взаимодействии ионов тяжелых металлов с водными растворами аммонийных солей без предварительного введения аммиака в раствор, если соль аммония сильно гидроли-зована. При этом образование аммиаката ускоряется в результате гидролиза. [1]
Образование аммиакатов наблюдается при адсорбции NH3 на CuNaY цеолитах. Однако эта адсорбция приводит к несколько отличающимся результатам в случае гидратированных и дегидратированных цеолитов. В атмосфере аммиака гидратированные цеолиты очень быстро приобретают интенсивную голубую окраску. Повышение энергии d - d переходов объясняется вхождением аммиака в координационную сферу ионов меди в CuNaY цеолитах. Аммиак в соответствии с его положением в спектрохи-мическом ряду [15] создает более сильное поле лнгандов, чем вода, что влияет на величину расщепления d - орбиталей, а следовательно, и на относительное положение полос поглощения в электронных спектрах соответствующих комплексов. [2]
Образование аммиаката стабилизирует у кобальта степень окисления ( III) и тем самым резко уменьшает возможность проявления комплексными соединениями кобальта ( III) окислительных свойств. [3]
Образование аммиаката приводит к хорошему разрешению всех довольно симметричных полос валентных колебаний. Частота валентного колебания связи C1N повышается на 27 - 88 см 1 по сравнению с v ( GlN) гидрата и безводной соли и может соответствовать ослаблению связи металл - азот пер-хлориламидогруппы при координации молекул аммиака около атома серебра. [4]
Реакцию образования аммиаката меди можно записать и в таком виде: Си2 4МНз [ Си ( МН3) 4 ] 2 - При этом подразумевается, что комплексный ион образуется из отдельных негидрати-рованных ионов меди, находящихся в газообразном состоянии, и газообразного аммиака. Однако и при таком в принципе правильном подходе возникают трудности, связанные с тем, что не во всех случаях известны термодинамические свойства исходных веществ. Поэтому в настоящее время способность элементов к комплексообразованию определяют различными косвенными методами. Ниже дается качественное описание способности элементов к комплексообразованию по группам периодической системы. [5]
На образовании устойчивых аммиакатов основаны гидрометаллургические методы извлечения никеля и руд. [6]
 |
Электронные спектры поглощения ионов [ № ( ОН2 р ( /, [ Ni ( NH3 e ] 2 ( 2 и [ Ni ( en 3 ] 2 ( 3. [7] |
На образовании устойчивых аммиакатов основаны гидрометаллургические методы извлечения никеля из руд. [8]
 |
Электронные спектры поглощения ионов [ Ni ( OH2 6P ( I, [ Ni ( NH3 6P ( 2 и [ Ni ( en 3P ( 3. [9] |
На образовании устойчивых аммиакатов основаны гидрометаллургические методы. [10]
Например, образование аммиакатов теория Косселя объясняет взаимодействием между ионами металлов и отрицательно заряженным концом молекул аммиака. [11]
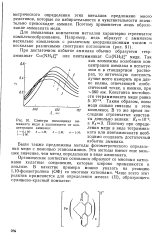 |
Спектры поглощения аммиаката меди в зависимости от концентрации аммиака. [12] |
Поэтому применяется лишь образование аммиаката меди. [13]
Возможность или невозможность образования аммиаката в каждом частном случае определяется соотношением величин Ez и Ег. В тех случаях, где Е1 очень велико, например у фторидов и окисей щелочных и щелочноземельных металлов, энергии, выделяющейся при взаимодействии катиона с аммиаком, оказывается недостаточно для перекрытия Elt и аммиакаты не образуются. [14]
Возможность или невозможность образования аммиаката в каждом частном случае определяется соотношением величин Ez и Ег. В тех случаях, где Ег очень велико, например у фторидов и окисей щелочных и щелочноземельных металлов, энергии, выделяющейся при взаимодействии катиона с аммиаком, оказывается недостаточно для перекрытия Et, и аммиакаты не образуются. [15]
Страницы: 1 2 3