Образование - аммин
Cтраница 1
Образование амминов в аммиачных растворах солей магния, кальция, бария, лития и калия было исследовано со стеклянным электродом. Было найдено, что в концентрированных водных растворах аммиака ион магния связывает до 6, ион кальция 4 - 6, ион лития 2 - 3 молекулы аммиака, в то время как в растворах солей бария и особенно калия, образование амминов совершенно незначительно. Значения ступенчатых констант, приведенные ниже, являются только ориентировочными, за исключением первой константы системы комплексов магния. [1]
Образование амминов в аммиачных растворах нитрата ртути ( II) было изучено при помощи стеклянного электрода. Было показано, что в этих растворах образуются только ам-мины, а гидроксо - и амидо-комплексы образуются в незначительном количестве. Обнаружено, что диамминовый комплекс ртути ( II) устойчив в широком интервале концентраций аммиака от 10 - 8 до 10 - 2, но при более высоких концентрациях аммиака этот комплекс довольно быстро превращается в тетр-аммин. [2]
Образование амминов в аммиачных растворах солей магния, кальция, бария, лития и калия было исследовано со стеклянным электродом. Было найдено, что в концентрированных водных растворах аммиака ион магния связывает до 6, ион кальция 4 - 6, ион лития 2 - 3 молекулы аммиака, в то время как в растворах солей бария и особенно калия, образование амминов совершенно незначительно. Значения ступенчатых констант, приведенные ниже, являются только ориентировочными, за исключением первой константы системы комплексов магния. [3]
Образование амминов в аммиачных растворах нитрата ртути ( II) было изучено при помощи стеклянного электрода. Было показано, что в этих растворах образуются только ам-мины, а гидроксо - к амидо-комплексы образуются в незначительном количестве. Обнаружено, что диамминовый комплекс ртути ( II) устойчив в широком интервале концентраций аммиака от 10 - 8 до 10 - 2, но при более высоких концентрациях аммиака этот комплекс довольно быстро превращается в тетр-аммин. [4]
Для К характерно образование амминов и др комплексных соединений Сухие соли К поглощают большие кол-ва МН3 - до 6 молекул на 1 мотекулу соли и более Гидроксид Се ( ОН) 2 растворяется в р-рах МН3 с образованием ионов [ Се ( МН3) 4 ] 2, при действии МН3 на р-ры солей К. [5]
Самые ранние исследования образования амминов в аммиачных растворах цинка и кадмия, а также образования ионов амминов металлов вообще относятся к рубежу двух столетий. Это было в то время, когда Коновалов [1] и Гауе [2], а также Досон и Мак-Крей [3] измерением упругостей пара аммиака и опытами по распределению смогли показать, что тетраммино-вый комплекс преобладает в аммиачных растворах как цинка, так и кадмия. [6]
Поскольку способность к образованию амминов увеличивается в ряду от бария к магнию, можно ожидать весьма значительное образование амминов в аммиачных растворах бериллия. [7]
Необходимость присутствия воды для образования аммина проявляется и в отношении фтористого кобальта к пиридину. [8]
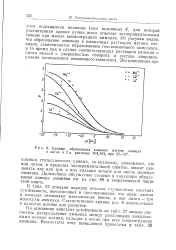 |
Кривые образования амминов магния, кальция и лития в 2 н. растворе NH4NO3 при 22 - 23. [9] |
Из рисунка видно, что образование амминов в аммиачных растворах магния, очевидно, заканчивается образованием гексамминового комплекса, в то время как в случае соответствующих растворов кальция и лития нельзя с уверенностью говорить о составе координационно насыщенного амминового комплекса. [10]
Из таблицы ясно, что образование амминов происходит настолько слабо, что неисправленные значения функции образования даже несколько отрицательны. Исправленные значения, по-видимому, показывают, что константа устойчивости, которую Жоб вычислил для комплекса моноамминталлия ( I), имеет правильный порядок величины. [11]
Исследование сильно облегчается, если образование амминов начинается при достаточно малой концентрации ионов гид-роксила, когда гидроксо-соединения образуются лишь в незначительных количествах. В большинстве случаев такое условие выполняется при достаточно высокой концентрации ионов аммония. Если акво-ионы металла имеют явно кислотный характер, необходимо принимать во внимание образование гидроксо-соединений. Для большинства одно - и двухзарядных ионов металлов кислотный характер не имеет большого значения. Однако кислотный характер трехзарядных ионов настолько ярко выражен, что гидроксо-соединения образуются в больших количествах, вследствие чего исследование образования амминов обычно становится невозможным. Кроме того, в отдельных случаях необходимо учитывать образование амидо-комплексов, например в системах аммиачных комплексов ртути и платины. [12]
 |
Кривые образования амминов магния, кальция и лития в 2 н. растворе NH4NO3 при 22 - 23. [13] |
Из рисунка видно, что образование амминов в аммиачных растворах магния, очевидно, заканчивается образованием гексамминового комплекса, в то время как в случае соответствующих растворов кальция и лития нельзя с уверенностью говорить о составе координационно насыщенного амминового комплекса. [14]
Из таблицы ясно, что образование амминов происходит настолько слабо, что неисправленные значения функции образования даже несколько отрицательны. Исправленные значения, по-видимому, показывают, что константа устойчивости, которую Жоб вычислил для комплекса моноамминталлия ( I), имеет правильный порядок величины. [15]
Страницы: 1 2 3