Образование - жидкость
Cтраница 2
Для предотвращения образования жидкости в турбодетандере может быть предусмотрена система защиты, которая при недопустимом понижении температуры входящего в него воздуха подает вначале сигнал, а затем прекращает подачу воздуха. [16]
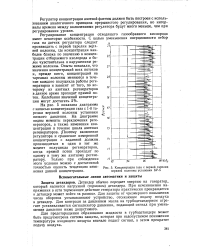 |
Концентрация газа с первой тарелки верхней колонны установки БР-5. [17] |
Для предотвращения образования жидкости в турбодетандере может быть предусмотрена система защиты, которая при недопустимом понижении температуры входящего воздуха вначале подаст сигнал, а затем прекратит подачу воздуха. [18]
В точке С образование жидкости прекращается, и поэтому эта точка называется критической. [19]
Эти силы способствуют образованию жидкостей и молекулярных кристаллов и увеличивают скорость химических реакций между молекулами. [20]
При температуре выше критической образование жидкости уже ни при каких давлениях невозможно. [21]
При температуре выше критической образование жидкости уже ни при каких давлениях невозможно. При температуре выше критической, например при 48 Г С ( рис. 79), изотерма углекислоты качественно выглядит так же, как изотермы идеального газа. [22]
Бесцветная гуанилтиомочевина плавится с образованием бледножелтой жидкости, которая при охлажлении вновь затвердевает и дает желтую кристаллическую массу; при плавлении происходит частичная перегруппировка в тиоцианат гуанидина. [23]
Продукт плавится при 1465 с образованием зеленой жидкости, которая затем быстро буреет и разлагается. [24]
Они плавятся при 625 с образованием жидкости темного цвета, трудно растворяются в полисульфидах щелочных металлов и в аммиаке и легко - в расплавленном едком кали. [25]
Признаком конгруэнтного плавления твердого вещества является образование жидкости того же химического состава. [26]
Плавление - итого соединении приводит к образованию жидкости совпадающего с ним состава и - называется конгруэнтным плавлением. Все ранее приводившиеся в этой главе примеры систем относится к этому типу. [27]
В процессе конденсации водяного пара с образованием жидкости или кристалла строение молекулы Н2О существенно не меняется. Характерные свойства конденсированных фаз определяются взаимодействием мономерных молекул. Результаты, полученные при изучении этих взаимодействий, будут описаны в последующих разделах. Отметим, что равновесные агломераты, состоящие из нескольких молекул воды ( до восьми в одной группе), были недавно детально изучены [66] на основе видоизмененной и расширенной теории молекулярных орбиталей Хкжкеля. [28]
В воде очень легко растворим с образованием прозрачной темно-желтой жидкости, которая в отличие от Na2S4 при нагревании темнеет лишь в малой степени: Na2S2 плохо растворим в холодном этиловом спирте. [29]
Заметим, что при изотермическом уменьшении объема образование жидкости начинается в точке пересечения изотермы с ветвью пара. [30]
Страницы: 1 2 3 4