Образование - кристаллический зародыш
Cтраница 2
При выполнении указанных условий столкновение молекул ( или ионов) приводит к образованию коротких цепей или плоских молекулярных слоев. Превышение сил взаимного притяжения над силами взаимного отталкивания приводит к образованию кристаллического зародыша, являющегося элементарной частицей твердого вещества. Устойчивое состояние частицы связано с ее размерами. [16]
Нерастворимые примеси, находящиеся в жидкости в мелкодисперсном состоянии, обычно понижают работу Лкр, необходимую для образования кристаллического зародыша, и служат центрами кристаллизации. Иногда наблюдается противоположный эффект, который объясняется затруднением процесса доставки молекул вещества через слой адсорбированной примеси к поверхности кристаллического зародыша. Растворимые примеси, влияющие на скорость кристаллизации, называются модификаторами. Применение модификаторов позволяет регулировать процесс кристаллизации и облегчает получение твердых веществ заданной структуры и с необходимыми свойствами. [17]
С помощью уравнения (XIX.19) можно объяснить влияние на кристаллизацию добавок посторонних веществ, с помощью которых изменяют скорость кристаллизации и выбирают необходимую для кристаллизации величину переохлаждения. Нерастворимые примеси, находящиеся в жидкости в мелкодисперсном состоянии, обычно понижают работу Лкр, необходимую для образования кристаллического зародыша, и служат центрами кристаллизации. Иногда наблюдается противоположный эффект, который объясняется затруднением процесса доставки молекул вещества через слой адсорбированной примеси к поверхности кристаллического зародыша. Растворимые примеси, влияющие на скорость кристаллизации, называются модификаторами. Применение модификаторов позволяет регулировать процесс кристаллизации и облегчает получение твердых веществ заданной структуры и с необходимыми свойствами. [18]
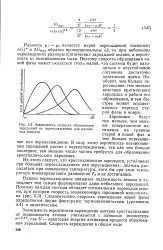 |
Зависимость скорости образования зародышей от переохлаждения для различных веществ. [19] |
В силу этого вероятность возникновения зародышей растет с переохлаждением, так как чем больше последнее, тем меньше число частиц требуется для образования кристаллического зародыша. [20]
Одни объясняют это с термодинамической точки зрения [112], исходя из работы образования равновесного зародыша, которая, как известно, равна 1 / 3 его поверхностной энергии. Термодинамические расчеты показывают, что при определенных условиях соотношений поверхностных натяжений менаду раствором и образующимся кристаллом, раствором и стенкой, новой фазой и стенкой работа образования кристаллического зародыша на стенке может оказаться значительно меньше работы образования его в растворе. Это облегчает процесс кристаллизации именно на стенке, а следовательно, приводит к образованию на ней устойчивых отложений. [21]
Некоторые авторы [25, 44] подходят к вопросу с чисто термодинамической точки зрения, используя представления Гиббса о поверхностной энергии раздела трех фаз, находящихся в контакте. Они считают, что в случае, когда контактный угол между кристаллическим осадком и поверхностью твердой частицы ( соответствующей краевому углу смачивания для систем жидкость - твердое тело) меньше 180, работа образования кристаллического зародыша на примеси меньше работы образования зародыша в объеме раствора и, следовательно, механические примеси будут увеличивать вероятность образования зародышей. [22]
Химическую поляризацию можно ослабить прибавлением веществ, активно взаимодействующих с веществами, ее вызывающими. Так, для поляризации, обусловленной выделением водорода на катоде, деполяризаторами могут служить различные окислители, а для уменьшения поляризации при выделении кислорода на аноде деполяризаторами могут служить различные восстановители. Фазовой поляризацией называется поляризация, связанная с процессом образования новой фазы - образования кристаллического зародыша. [23]
Рассматривая путь иона из гидратированного состояния в растворе до кристаллического состояния на катоде, Фольмер указывает, что получившиеся после разряда атомы должны принять в металле ориентированное положение. И даже в том случае, если разряд ионов совершается беспрепятственно на любых участках электрода, то стадия образования и роста кристаллов может оказаться замедленной. Исходя из предпосылки, что процесс электрокристаллизации является частным случаем фазовых превращений при образовании кристаллического зародыша внутри газообразной фазы, или расплава, Фольмер полагает, что плотность тока здесь играет такую же роль, как пересыщение при кристаллизации из раствора или величина температурного градиента при кристаллизации из расплава. При фазовых превращениях одна фаза может перейти в другую или путем возникновения зародышей новой фазы внутри прежней, или, если эти процессы не связаны с образованием зародышей, в результате удаления поверхностных атомов твердого тела. [24]
Пересыщенные растворы часто образуют вещества со сложной конфигурацией молекул. Хлорид серебра выпадает в осадок из пересыщенных растворов очень быстро, так как Ag и С1 - имеют сферическую форму и легко образуют центр кристаллизации. В противоположность этому ацетат натрия склонен к образованию пересыщенных растворов ввиду того, что низкая симметрия ацетатного иона затрудняет образование кристаллического зародыша. [25]
Пересыщенные растворы часто образуют вещества со сложной конфигурацией молекул. Хлорид серебра выпадает в осадок из пересыщенных растворов очень быстро, так как Ag и С1 - имеют сферическую форму и легко образуют центр кристаллизации. В противоположность этому ацетат натрия склонен к образованию пересыщенных растворов, ввиду того, что низкая симметрия ацетатного иона затрудняет образование кристаллического зародыша. [26]
Согласно существующим представлениям, образование твердой фазы начинается с возникновения зародышей. Одни авторы2 считают, что первичным актом образования твердой фазы является возникновение кристаллического зародыша. Кристаллические зародыши образуются в результате некоторого пересыщения раствора, возникающего при введении реагентов в рассол, а также вследствие флуктуации тепла или массы растворенного вещества. Для образования кристаллического зародыша необходима такая ориентировка ионов или молекул, которая соответствует их положению в кристаллической решетке данного вещества. Вероятность создания таких условий зависит от концентрации и скорости диффузии вещества. [27]
 |
Диаграмма состояния системы лейцит-форстерит-селлаит. [28] |
Механизм влияния растворенных газов на физико-химические свойства окисных расплавов связан с формой их существования в последних. Растворение азота вызывает увеличение вязкости по отношению к среде аргона, поскольку атомы азота связываются с катионами в расплаве, уменьшая их подвижность. Растворение в силикатном расплаве водородсодержащих газов Н2О, Н2, NH3 понижает поверхностное натяжение ( по отношению к Аг), а растворение N2 повышает его. Поскольку работа образования кристаллического зародыша тем больше, чем больше поверхностное натяжение, растворение разов облегчает ( Н2) или затрудняет ( N2) зароды шеобразование в расплаве. [29]
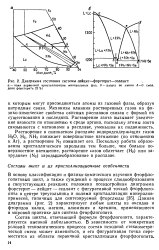 |
Диаграмма состояния системы лейцит-форстерит-селлаит. [30] |
Страницы: 1 2 3