Образование - анион
Cтраница 1
Образование анионов происходит в результате присоединения электрона к атому. Мерой способности к такому присоединению служит так называемое сродство к электрону. [1]
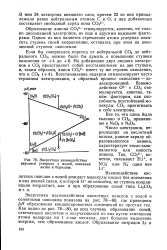 |
Энергетика взаимодействия двуокиси углерода с водой, окислами. [2] |
Образование аниона СО32 - стимулируется, конечно, не только диссипацией электронов, но еще и другими важными факторами. Одним из них является стремление атома углерода повысить ступень своей координации, оставаясь при этом на неизменной ступени окисления. [3]
Образование аниона BF4 - сопровождается некоторым уменьшением радиуса аниона по сравнению с В03 - - и падением его заряда с 3 - до 1 -, что приводит к резкому уменьшению плотности заряда на поверхности аниона. В то же время радиус BF4 - значительно больше радиуса F - в анионе плавиковой кислоты. [4]
Образование анионов гидроксила из кислорода, требующее присоединения к нему электронов, является процессом восстановления кислорода. Обратный процесс - превращение анионов гидроксила в кислород - является окислением. [5]
Образование аниона псевдокислоты является самой медленной стадией превращения, определяющей ее общую скорость; в кинетическое выражение входит только концентрация метиленовой, но не карбонильной компоненты. [6]
Образование возбужденных анионов фенолов в нейтральной среде связано с уменьшением рК в возбужденном состоянии. [7]
Образование аниона уксусного ангидрида; основанием служит уксуснокислый натрий. [8]
Образование бесцветных клещевидных анионов с органиче-кими кислотами ( лимонная, винная, салициловая) имеет боль-цое значение для маскировки присутствия ионов А13, Fe3, Cr3 j растворе, а в том случае, когда они окрашены, как салицилат келеза, - для открытия их. [9]
Объяснение образования анионов наличием более высокого КЧ по сравнению с ЧС имеет значение только в той мере, в какой возможно приписать Л - частицам вероятные КЧ и вывести координационные свойства их из строения атома. В общем это действительно имеет место ( хотя и не во всех подробностях), причем ( так же как и в отношении валентностей) у известных электроположительных частиц различные КЧ могут конкурировать между собой. [10]
Объяснение образования анионов наличием более высокого КЧ по сравнению с ЧС имеет значение только в той мере, в какой возможно приписать А-частицам вероятные КЧ и вывести координационные свойства их из строения атома. [11]
Реальность образования аниона I подтверждается тем, что оптически активные сложные эфиры рацсмизуются в присутствии этилата натрия, а также тем, что скорость К. Рейтером и подробно изучена в 1887 Клай-зеном. [12]
Медленная стадия образования аниона определяет скорость процесса в целом. Если R - не способен к существованию, то обмен Н на D не происходит. Экспериментально показано, что циклопро-пены, содержащие при атоме углерода электроотрицательные группы ( СО, C N), вступают в реакцию обмена, но крайне медленно, что указывает на исключительно малую стабильность промежуточно образующегося аниона. [13]
Медленная стадия образования аниона определяет скорость процесса в целом. [14]
Скорость реакции образования аниона кетоепола ( соответственно, константа скорости к) мала. [15]
Страницы: 1 2 3 4