Образование - первичный ион
Cтраница 1
Образование первичного иона в результате присоединения мономера по связи металл-углерод в металлорганическом соединении легко наблюдать прк полимеризации бутадиена в присутствии фенилизопропилкалия. Последний имеет ярко-красную окраску, обусловленную связью калия с фенильной группой угле водородного радикала. После введения бутадиена в эфирны. Полимеризацию бутадиена обычно проводят в присутствии металлического натрия. [1]
После образования первичных ионов и возбужденных молекул может протекать целый ряд вторичных процессов, прежде чем произойдут химические изменения. Среди таких процессов возможны следующие: передача возбуждения и ионизации между одинаковыми и разными молекулами, нейтрализация ионов, образование отрицательных ионов и радикал-ионов. К настоящему времени уже изучен целый ряд химических изменений, происходящих под действием ионов и свободных радикалов, образованных в системе указанным выше способом. [2]
В связи с частыми соударениями ионов и молекул в процессе образования первичных ионов газа-реактанта происходит выравнивание энергий, в связи с чем энергетичность QM невелика. [3]
Ионы, образующиеся на последовательных ступенях распада молекулярного иона, позволяют установить механизм образования первичных ионов, которые очень часто являются перегруппировоч-ными. [4]
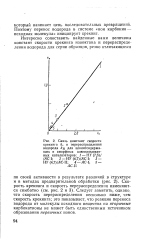
Величина темнового тока, обычно не превышающая один микроампер, заклеит от скорости образования первичных ионов и от скорости их отвода. Первое связано с интенсивностью ионизирующего излучения, второе - с величиной напряжения U между электродами. Зависимость между напряжением и темновым током представлена графически участком Оаб на рис. 2.18. Постоянство величины темнового тока на участке аб показывает, что уже в точке а скорость отвода первичных ионов становится равной скорости их образования. [5]
Диметилбутены, образованные по схеме ( Па), могут в свою очередь давать 2-метилпентены ( Пб) через стадии, которые включают образование нестабильного первичного иона карбония. Следовательно, превращение по схеме ( Пб) должно протекать медленнее, чем ( Па), или требовать более сильных кислотных центров. По аналогичным причинам конверсия 2-метилпентенов в гексены ( Иг) также протекает медленно. Следовательно, важна не только общая конверсия 3 3-диметилбутена, но также и глубина изомеризации. [6]
Следует заметить, однако, что скорость перераспределения несколько ниже, чем скорость крекинга; это показывает, что реакция переноса водорода от молекулы исходного вещества на вторичные карбокатионы не может быть единственным источником образования первичных ионов. [8]
Отсюда следует, что образование первичного иона гексадоцила путем переноса гидридного иона в данном случае маловероятно, поскольку для этой эндотермической реакции потребовалась бы теплота порядка 266 0 - 249 5 16 5 ккал / молъ. [9]
Расчеты [9] i показывают, что теплота образования первичных карбениевых ионов на 81 кДж / моль больше, чем для втр-ричных, а теплота образования вторичных ионов на 61 кДж / моль больше, чем для третичных, вследствие чего в это же последовательности возрастает стабильность ионов. Вследствие этого предполагается, что первичные карбениевые ионы быстро - переходят в третичные или непредельные ионы, а при превращениях последних образование первичных ионов мало вероятно. [10]
Как и в предыдущем случае, происходит перенос гидрид-иона от молекулы алкана на этот карбокатион. Рассмотренные здесь модификации протонного и апро-тонного механизмов несколько расширяют круг опытных данных, интерпретируемых в рамках карбоний-ионной теории; однако и они не универсальны. По-видимому, наиболее близким к действительности является осторожное утверждение Жермена [5]: ни один из указанных механизмов не может быть единственным, ответственным за образование первичных ионов карбония при превращениях алканов. [11]
Крекинг и изомеризация парафиновых углеводородов являются важнейшими промышленными процессами, но механизмы реакций, составляющих основу этих процессов, изучены явно недостаточно. Наиболее просто было бы предположить, что определенные активные центры цеолитов способны непосредственно разрывать связи С - Н или С - С, тем более, что в гомогенных системах подобные процессы наблюдаются. Однако до сих пор мы не располагаем надежными данными о том, что такие процессы могут конкурировать с процессом образования ионов карбония путем протонирования олефинов и последующего отрыва гидрид иона. Наиболее подробно реакции крекинга изучены на примере парафиновых углеводородов С4 и С5, хотя на самом деле эти молекулы занимают особое положение, так как у них прямое расщепление С - С-связей неизбежно должно привести к образованию первичных ионов карбония, что связано с преодолением высокого энергетического барьера. Наконец, можно отметить, что для крекинга на цеолитах очень характерна реакция перераспределения водорода, которая по всей вероятности протекает путем гидридного переноса. [12]
Страницы: 1