Образование - карбонат
Cтраница 3
Дальнейшее изложение относится главным образом к тем мощным образованиям карбонатов, называемых известняками, магнезиальными или доломитовыми известняками и доломитами, из которых многие имеют большое и все возрастающее экономическое значение. Даже у геологов нет определенных правил для строгого их разграничения, а из соотношения окислов следует, что всякое разграничение будет произвольным, так как известняки и доломиты образуют совершенно непрерывный ряд. [31]
Как и раньше, отравление катода обусловливается образованием карбонатов. Быстрый рост кривых при более низких температурах указывает на значительную температурную зависимость скоростей реакций. [33]
Другим неизбежным процессом, сопутствующим электролизу, является образование карбонатов. Содержание их в электролите допускается достаточно высоким - до 10 г / л, но переходить за этот предел не рекомендуется, поскольку наблюдается резкое падение концентрации металла в электролите, а аноды покрываются плотной серой пленкой. Для подавления реакции карбонизации в состав электролита вводится щелочь. В случае накопления избыточного количества карбонатов их следует удалять окисью бария из расчета 1 5 г на 1 г углекислых солей. После этого производится корректировка содержания щелочи. [34]
В качестве другого доказательства нашей точки зрения может рассматриваться экзотермическое образование карбонатов из окислов и двуокиси углерода, что мы, например, наблюдали при растирании окиси цинка в среде двуокиси углерода, ибо высокие температуры должны способствовать ходу реакции в противоположном направлении. На самом деле является недопустимым приписывать влияние высокой температуры каждому возбужденному или активному состоянию определенных, особенно очень малых, участков пограничных поверхностей твердых веществ даже тогда, когда это состояние повышенной энергии вызвано механической работой. Предположение о действии тепла не выдерживает критики, особенно при механохимических реакциях, которые являются неизбежными при совершенно минимальном механическом воздействии на твердые вещества, как, например, образование сернистого железа при весьма осторожном смешивании порошков железа и серы или же взрывообразное разложение йодистого азота при легком касании. [35]
Вместе с тем в присутствии кислоты становится невозможным и образование карбонатов щелочноземельных металлов: как видно из табл. 8 и 9, во всех тех случаях, когда адсорбция производилась из подкисленных растворов, концентрация катионов кальция и стронция оставалась после опыта почти неизменной. [36]
При 0 0 не могут быть полностью исключены реакции образования карбоната и р-аминоэтилкарбоновой кислоты. Астарит а [12] приблизительно подсчитал, что вклад вторичных реакций повышается лишь при величине & хш - 5400 л / ( г-мол сек) при 21 5 С. [37]
Реакция может идти в двух направлениях: в направлении образования карбонатов в результате взаимодействия щелочи с углекислотой воздуха, то есть в направлении уменьшения прочности образцов, и в направлении образования силикатов, то есть в направлении увеличения их прочности. [38]
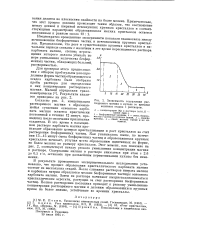 |
Зависимость содержания растворимого магния в пульпе от времени контакта осадка с раствором. [39] |
В результате проведенного экспериментального исследования установлено, что процесс образования кристаллического карбоната магния состоит из нескольких стадий. После сливания растворов нитрата магния и карбоната натрия образуются мелкие бесформенные частицы основного карбоната магния. Затем из раствора начинают выкристаллизовываться кристаллические агрегаты, растущие за счет растворения бесформенных частиц. Полное растворение последних приводит к резкому уменьшению концентрации растворимого магния и делению образовавшихся крупных призм на более мелкие, устойчивые во времени кристаллы. [40]
Относительно высокая основность редкоземельных элементов доказывается их способностью к образованию карбонатов. Кристаллические карбонаты получаются при пропускании углекислоты в суспензию гидроокисей или посредством добавления щелочного карбоната к нейтральным растворам солей редкоземельных элементов. Растворимость карбонатов в углекислом аммонии увеличивается параллельно с ростом атомного номера редкоземельного элемента. Двойные карбонаты как натрия, так и аммония менее растворимы, чем соответствующие соединения калия, и это обстоятельство часто используется в методах фракционной кристаллизации. [41]
Эти нерастворимые продукты при нагревании на воздухе разлагаются с образованием карбонатов, причем растворимые карбонаты рубидия и цезия можно из продуктов разложения выщелачивать водой. [42]
При этом аммиачный комплекс разрушается с выделением аммиака и образованием карбоната кадмия. [43]
Реакция между углекислым газом и водным раствором щелочи с образованием карбонатов щелочных металлов представляет собой основу оригинальной системы детектирования, первоначально разработанной Янаком. Низкомолекулярные углеводороды элюируют с колонки углекислым газом и смесь газов собирают в бюретку, заполненную раствором едкого натра. Газ-носитель поглощают количественно, а легкие углеводороды собирают над жидкостью и измеряют объемным методом. [44]
 |
Действие некоторых реактивов на катионы II аналитической группы. [45] |
Страницы: 1 2 3 4