Образование - карбонат - кальций
Cтраница 2
Запись данных опыта, Отметить наблюдаемые явления и на - писать уравнения реакции: образования карбоната кальция при взаимодействии диоксида углерода с известковой водой и растворения карбоната кальция под действием диоксида углерода и воды с образованием гидрокарбоната. [16]
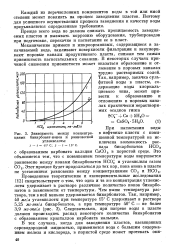 |
Зависимость между концентрациями бикарбонат-ионов и равновесной углекислоты. [17] |
При нагнетании воды в нефтяные пласты с повышенной температурой не исключена возможность распада бикарбонатов НС03 с образованием карбоната кальция СаС03 в пористой среде. Проведенные теоретические и экспериментальные исследования [12] свидетельствуют о том, что одна и та же концентрация углекислоты удерживает в растворе различное количество ионов бикарбонатов в зависимости от температуры. Чем выше температура раствора, тем в ней меньше удерживается бикарбонатов. Следовательно, при нагреве воды в пласте должен происходить распад некоторого количества бикарбонатов с образованием кристаллов карбоната кальция. [18]
При длительном соприкосновении с воздухом часть гидроокиси кальция взаимодействует с содержащейся в воздухе двуокисью углерода с образованием карбоната кальция. [19]
При нагнетании холодной воды в нефтяные пласты с повышенной: температурой не исключена возможность распада бикарбонатов и образования карбоната кальция ( СаС03) в пористой среде. Проведенные теоретические и экспериментальные исследования [13] свидетельствуют о том, что при одной и той же концентрации С0а в растворе удерживается различное количество ионов бикарбоната в зависимости от температуры раствора. [20]
При прокаливании угля со смесью Эшка сульфат кальция и пирит прореагируют с содой при накаливании в сторону образования карбоната кальция, сульфата натрия и сернистого натрия. При накаливании смеси Эшка с углем сульфат натрия может сполна или отчасти восстановиться до сернистого натрия. [21]
При подкислении воды выделяется свободная углекислота, которая, находясь в равновесном состоянии с гидрокарбонатами, препятствует образованию карбоната кальция и, следовательно, отложению его на стенках трубопроводов при подаче воды потребителю. [22]
Также не рекомендуется использовать минерализованные растворы, содержащие кальций, в условиях возможного поступления углекислого газа во избежание образования карбоната кальция с последующим выпадением его в осадок. [23]
 |
Модель опыта М. Ломоносова. горение свечи на весах в замкнутом пространстве. [24] |
Затем в колбу налить 10 - 20 мл прозрачной известковой воды и встряхнуть - жидкость мутнеет в результате образования карбоната кальция. Это указывает на наличие второго продукта горения свечи - диоксида углерода. [25]
При обсуждении метода удаления фосфата обработкой известью Меррим и Джорден отмечают, что фосфат удаляется лучше, если процесс образования карбоната кальция ингиби-рован. К сожалению, эти авторы использовали неточные значения растворимости карбоната кальция, который образуется в результате добавления извести к сточным водам. Тем не менее они сделали вывод, что для характеристики реакций осаждения, вызванных добавками извести, могут быть использованы равновесные модели или модели неизменного состояния. Как будет показано ниже, использование таких моделей для расчета процесса образования карбоната кальция в сточных водах может привести к большим ошибкам. Так, обычные концентрации определенных примесей, например фосфата, могут снизить константу скорости образования карбоната кальция па несколько порядков к быть причиной успешной или неудачной обработки сточной воды известью. [26]
Для определения возможности удовлетворительной очистки сточной воды в каждом конкретном случае должны быть тщательно оценены кинетические факторы, влияющие на образование карбоната кальция. Данный кинетический фактор исследован недавно. [27]
При подкислении щелочность воды понижается и выделяется свободная углекислота, которая, находясь в равновесном состоянии с гидрокарбонатами, препятствует образованию карбоната кальция и, следовательно, зарастанию трубопроводов при подаче воды потребителю. [28]
Те же микробиологические процессы, которые способствуют восстановлению в морских осадках соединений железа и серы, могут вызвать в этих осадках образование карбоната кальция. Поэтому помимо закисных и окисных форм железа и серы была определена карбонатность осадков. [29]
Са ( ОН) 2 следует прибавить к 162 г 5 % - ного раствора Са ( НСО3) 2 для образования карбоната кальция. [30]
Страницы: 1 2 3 4