Образование - катализатор
Cтраница 2
После растворения натрия через раствор пропускают в течение приблизительно 1 5 мин воздух для образования катализатора, который должен способствовать быстрому превращению металлического натрия в амид. Затем добавляют в несколько приемов все необходимое количество металлического натрия ( всего 1 17 моль, или приблизительно 27 г) при непрерывном перемешивании. Реакция протекает интенсивно, с выделением водорода. [16]
Было высказано предположение [11], что между металлом и углеродом происходит специфическое взаимодействие с образованием катализатора, обладающего значительно большей активностью, чем каждый из компонентов в отдельности. На металле без носителя образуется мало твердого полимера, а на угле, обработанном азотной кислотой, полимеризация совсем не идет. По-видимому, указанное взаимодействие способствует благоприятному расположению центров адсорбции мономера и тем самым контролируемому росту цепи, приводящему к образованию твердого полимера. [17]
В 1929 г. была опубликована работа Андерсона [27], в которой указывалось, что сочетание металлов приводит к образованию более деятельных катализаторов, чем те же металлы, взятые порознь. Это положение сохраняет свое значение и для квазигетерогенных катализаторов. [18]
Комбинации, состоящие из окислов элементов других пар типов или одного и того же типа, должны привести к образованию катализаторов, не обладающих заметной активностью в этой реакции. [19]
Комбинации, состоящие из окислов элементов других пар типов или одного и того же типа, должны привести к образованию катализаторов, не обладающих заметной активностью в этой реакции. [20]
СО на реакцию и образование катализатора, м3 / ч; 1 / н - общий расход Н2 на реакцию и образование катализатора, м3 / ч; со с о - содержание СО в техническом оксиде углерода и техническом водороде соответственно, мольн. [21]
Состав твердой фазы катализатора А1 ( С2Нб) з - TiCl 4 зависит от того, как прибавляли металлоорганический компонент во время образования катализатора - сразу или по частям. В соответствии с этим изменение состава катализатора, полученного из Al ( C2Hs) 3, как функции молярного соотношения Al / Ti не является результатом равновесной реакции. [22]
Наиболее вероятный механизм ускоряющего действия сероводорода представляется в следующем виде: на поверхности железного электрода происходит взаимодействие хемосорбированных ионов HS - с ионами НзО из раствора с образованием катализатора - молекулярного поверхностного комплекса Fe ( H-S - Н) адс Протоны этого комплекса при катодной поляризации восстанавливаются до атомов водорода, которые могут частично рекомбинировать, частично диффундировать в металлы, вызывая водородную хрупкость. [23]
На катализаторах Циглера получают линейные, высокомолекулярные, изотактические, кристаллические тюлимеры при полимеризации мономеров типа RR R Sn ( CH2) nCHCH2; полимеры взаимодействуют с галогенидами переходных металлов с образованием катализаторов полимеризации. [24]
Образующийся комплекс разлагается, и сероводород регенерируется. При образовании хемосорбировашюго катализатора Ре ( Н5 -) адс на поверхности металла прочная связь атомов железа с серой приводит к ослаблению связи между атомами металла, что и облегчает их ионизацию. При этом происходит сдвиг электродного потенциала железа в отрицательную сторону, что ведет к увеличению скорости анодного процесса коррозии. [25]
Образующийся комплекс разлагается, и сероводород регенерируется. При образовании хемосорбированного катализатора Fe ( Н8 -) адс на поверхности металла прочная связь атомов железа с серой приводит к ослаблению связи между атомами металла и облегчению их ионизации. [26]
Рогннский и О. М. Тодес [43] выяснили распределение по дисперсности кристаллических зародышей новой фазы в процессе их роста. Изучая процессы образования катализаторов - адсорбцнонно и химически активных дисперсных твердых тел, С. Рогпнскнй, А. Б. Шехтер и И. И. Третьяков [44] детально исследовали электронномпкроскопическн дисперсную структуру поверхности катализаторов и ее изменения в процессах катализа. [27]
Это наблюдение, как показали поставленные опыты, подтверждается при полимеризации пропилена в полипропилен. Рекомендуемый способ образования катализатора позволяет сохранить высокую активность каталитического комплекса в течение сравнимого длительного перепада времени. [28]
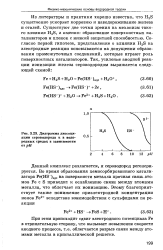 |
Диаграмма диссоциации сероводорода а в водородных средах в зависимости от рН. [29] |
Данный комплекс разлагается, и сероводород регенерируется. Во время образования хемосорбированного катализатора Ре ( Н8 -) адс на поверхности металла прочная связь атомов Fe с S приводит к ослаблению связи между атомами металла, что облегчает их ионизацию. [30]
Страницы: 1 2 3 4