Образование - комплексный катион
Cтраница 3
 |
Катодная и анодная ветви перенапряжения кадмия ( амальгама в отсутствие ( 1 и в присутствии соли тетрабутилам-мония ( 2. [31] |
Как мы упоминали выше, в некоторых случаях может иметь значение определяющее участие аниона в образовании комплексного катиона более низкой зарядности и, следовательно, менее гидратированного. [32]
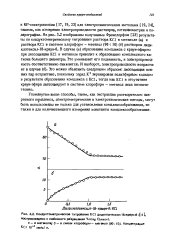 |
Кондуктометр ческое титрование КС1 дициклогексил-18 - краун-б ( [ 41 воспроизведено с любезного разрешения Verlag Chemie. [33] |
На рис. 3.2 изображены полученные Френсдорфом [23] результаты по кондуктометрическому титрованию раствора КС1 в метаноле ( ajf и раствора КС1 в системе хлороформ - метанол ( 90: 10) ( б) раствором дици-клогексцл-18 - краун-б. В рлучае ( а) образование комплекса с краун-эфиром при диссоциации КС1 в метаноле приводит к образованию комплексного катиона большего диаметра. Это уменьшает его подвижноть, и электропроводность соответственно снижается. Это можно объяснить оледуюшим образом: диссоциация ионных пар возрастает, поскольку заряд К экранирован полиэфирным кольцом в результате образования комцлекса с КС1, тогда как КС1 в отсутотвие краун-эфира диссоциирует в системе хлороформ - метанол лишь незначительно. [34]
 |
Кондуктометр ческое титрование КС1 дициклогексил-18 - краун-б ( [ 41 воспроизведено с любезного разрешения Verlag Chemie. [35] |
На рис. 3.2 изображены полученные Френсдорфом [23] результаты по кондуктометрическому титрованию раствора КС1 в метаноле ( а и раствора КС1 в системе хлороформ - метанол ( 90: 10) ( б) раствором дици-клогексил-18 - краун-6. В рлучае ( а) образование комплекса с краун-эфиром при диссоциации КС1 в метаноле приводит к образованию комплексного катиона большего диаметра. Это уменьшает его подвижноть, и электропроводность соответственно снижается. Это можно объяснить оледуюшим образом: диссоциация ионных пар возрастает, поскольку заряд К экранирован полиэфирным кольцом в результате образования комцлекса с КС1, тогда как КС1 в отсутотвие краун-эфира диссоциирует в системе хлороформ - метанол лишь незначительно. [36]
Fe ( OH) 2, Мп ( ОН) 2, Mg ( OH) 2 осаждаются не полностью, так как они частично растворимы в солях аммония. Гидроксиды цинка, меди, никеля, кобальта, кадмия и серебра растворимы в избыточном количестве водного раствора аммиака с образованием комплексных катионов - аммиакатов. [37]
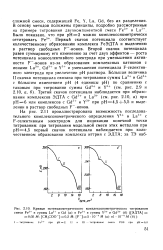 |
Кривые потенциометрического комплексонометрического титрования. [38] |
Первый скачок потенциала соответствует количественному образованию комплекса РеЭДТА и выделению в раствор свободных Р - - ионов. Второй скачок потенциала равен суммарному его изменению за счет двух эффектов - роста потенциала ионоселективйого электрода при уменьшении активности Р - - ионов из-за образования комплексных катионов с ионами La3, Gd3 и Y3 и уменьшения потенциала Р - селектив-ного электрода при увеличении рН раствора. Третий скачок потенциала наблюдается при образовании комплексов ЭДТА с Gd3 и La3 ( см. рис. 2.10, а) при рН 6 или комплексов с Gd3 и Y3 при pH4 5 - f - 5 5 и выделении в раствор свободных Р - - ионов. [39]
Диантипирилметан нельзя рассматривать как азотистое основание. Из его строения, а также по инфракрасным спектрам его комплексов очевидно, что при образовании солей с простыми анионами или анионными комплексами металлов или при образовании комплексных катионов аминного типа значительную роль играют С О-группы реактива. Тем не менее диантипирилметан близок по свойствам к типичным азотистым основаниям, строение которых способствует образованию координационных связей металл - азот. Антипирин, который является простым аналогом и исходным веществом для получения диантипирилметана, также способен к образованию комплексов обоих типов. [40]
Глицин был применен Головатовым и Ощаповским [2] при. Глициновые растворы были применены Зверевой [3] при катионообменном разделении ионов марганца, кальция и магния и было показано, что эти ионы в широком интервале значений рН раствора в присутствии глицина показывают постоянное значение коэффициентов распределения металла между катионитом и раствором, связанное с образованием однозарядных комплексных катионов. [41]
Образуется прозрачный раствор сине-фиолетового цвета. Исследованиями установлено, что в данном случае имеет место образование комплексного катиона [ Cu ( NH3) 4 ], образовавшегося путем присоединения к иону Си четырех молекул аммиака. Характерная окраска раствора вызвана образованием этого комплексного катиона. [42]
Страницы: 1 2 3