Образование - циклопропановое кольцо
Cтраница 1
Образование циклопропановых колец в мостиковых системах при сольволизе и аналогичных реакциях известно давно [58, 59, 139, 159, 187, 293, 317, 318] ( в некоторых случаях, правда, требуется подтверждение), но описанное выше превращение является, по-видимому, единственным примером участия метильной группы в такого рода превращении и к тому, же в немостиковой системе. Так как близкие по строению производные ( 5-амирина не претерпевают этого превращения [5], возможно, что одним из действующих факторов является стерическое сжатие между карбонилом при G-12 и метильной группой у G-19, ослабляемое при образовании мостика. Это интересное участие метильной группы является, по-видимому, результатом целого ряда особых условий. [1]
Поскольку образование циклопропанового кольца происходит через енольную форму исходного соединения, такие процессы называются еноленовымн перегруппировками или гомо - [1,5] - сигматропным сдвигом водорода. [2]
Одним из старейших методов образования циклопропанового кольца является пиролиз 1-пиразолинов. Пира-золины получают обычно реакцией между олефинами идиазосоединениями. Однако существует также ряд способов, при использовании которых возможно проводить реакцию между олефинами и диазосоединениями таким образом, что в результате сразу образуются циклопропаны. [3]
Например, предполагается, что в нормальных парафинах происходит образование циклопропанового кольца, в результате чего заряд, по-видимому, не расплывается и остается в области столкновения вплоть до распада. В масс-спектрах таких веществ обычно можно четко различить две группы ионов: характерные для алка-нов и характерные для данной функциональной группы. [4]
Арильная группа перемещается строго стереоеелективно и, возможно, синхронно с образованием циклопропанового кольца. У ал-кильных групп склонность к перемещению столь незначительна, что у 4 4-диалкилциклогексенонов перегруппировка типа XXII - - - XXIII не имеет места. В этом случае получаются 3 3-диалкил - 2-циклопентеноны. [5]
Эта величина сравнима со значением 10 ккал / моль, которое необходимо для образования циклопропанового кольца из 1 3-бирадикала. Таким образом, полученное значение кажется вполне приемлемым. Условием быстрой инверсии является неравенство Ет 8 9 ккал / моль. Для циклогексана методом ЯМР получено значение высоты барьера инверсии, равное 10 ккал / моль. Для цикло-пентанов эта величина должна быть заметно меньше, так как у них возможно быстрое псевдовращение, приводящее к инверсии цикла. Применив метод стационарных концентраций для расчета скорости образования циклопентена, получим, что энергия активации ( Ес) миграции водорода в бирадикале ( реакция с) равна 16 6 ккал / моль, а не 11 ккал / моль, как в триметиленовом бирадикале. Это можно объяснить тем, что в переходном состоянии этой реакции четыре атома углерода, образующие цикл, должны лежать в одной плоскости, и поэтому наблюдаемая величина энергии активации характеризует не только миграцию водорода, но и инверсию цикла. Таким образом, для инверсионного барьера может быть получено вполне допустимое значение 5 ккал / моль. [6]
Обычно - элиминирование приводит к тому же продукту, что и р-элиминирование, но в первом случае возможно также образование циклопропанового кольца, если алкилгалогенид имеет разветвленную цепь. [7]
Обработка поливгшилхлорида литием или калием также приводит к образованию металлированиого полимера, в котором остается еще немного хлора и имеет место образование циклопропановых колец и спшвка. [8]
Обработка поливжнилхлорида литием или калием также приводит к образованию металлированного полимера, в котором остается еще немного хлора и имеет место образование циклопропановых колец и сшивка. [9]
В обоих случаях, как в соединении ( 2), так и в ( 4), преимущественно разрывается циклопропановая связь, несущая два фе-нильных заместителя; и при этом генерируется радикал-анион, атакующий затем ближайшую С-0-связь с образованием нового циклопропанового кольца. Циклопропановые кольца в соединениях ( 3) и ( 5), по-видимому, защищены от дальнейшего восстановления электростатическими факторами. [10]
В обоих случаях, как в соединении ( 2), так и в ( 4), преимущественно разрывается циклопропановая связь, несущая два фе-нильных заместителя; и при этом генерируется радикал-анион, атакующий затем ближайшую С-0-связь с образованием нового циклопропанового кольца. Циклопропановые кольца в соединениях ( 3) и ( 5), по-видимому, защищены от дальнейшего восстановления электростатическими факторами. [11]
Аналитические способы определения очень небольших количеств таких структур, понижающих термическую устойчивость полимеров, еще недостаточно точны. Один из приемов идентификации основан а взаимодействии заместителей друг с другом с образованием циклопропанового кольца. [12]
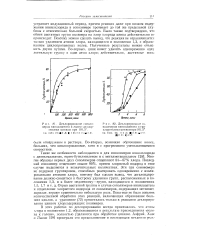 |
Дехлорирование сополимеров винилацетата и транс-дихлор.| Дехлориропание сополимеров винилацетата и три-хлорэтилена цинком при 101 5. [13] |
Было также подтверждено, что обмен ацетатных групп полимера на хлор хлорида цинка действительно не происходит. Поэтому можно сделать вывод, что реакция не ограничивается только удалением атомов хлора, находящихся в положении 1 3, с образованием циклопропановых колец. [14]
Карбен: СН2, образующийся при индуцируемом светом разложении диазометана, - один из наиболее реакционноспособных реагентов, известных в органической химии. Можно осуществить более селективные реакции карбе-нов ( получая последние путем отщепления йодистого цинка из йодистого иодметшщинка ICH2ZnI), которые в случае простых алкенов приводят только к образованию циклопропанового кольца. [15]
Страницы: 1 2