Образование - комплекс - тип
Cтраница 1
Образование комплекса типа ThR, в котором группа As03H2 двухфункциональна, должно сопровождаться выделением трех ионов водорода, причем один из них выделяется за счет образования связи металла с оксигруппой молекулы. [1]
Для образования комплекса типа КОН ( Н202) необходимо наличие определенного соответствия между расстоянием К-О в частице КОН и расстояниями О-О и ОН в молекуле перекиси водорода. По-видимому, в соединениях титана и ванадия расстояния Ti-О и V-О оказываются слишком малыми для образования устойчивого пероксоцикла и по этой причине титан и ванадий не обладают каталитической активностью в реакции окисления иодид-ионов перекисью водорода. [2]
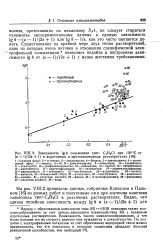 |
Зависимость gk сольволиза трет - С4Н9С1 при 120 С от ( е - 1 / ( 2е 1 в апротонных и протонодонорных растворителях. [3] |
Наряду с образованием комплексов типа RX HOR возможно также ком-плексообразорание за счет диполь-дипольного взаимодействия RX с полярным апротонным растворителем. Возможность такого комплексообразования, а тем более влияние его на скорость реакции еще нуждаются в доказательстве. По аналогии с электрофильным катализом за счет образования водородной связи можно предположить, что эти комплексы в реакциях сольволиза обладают большей реакционной способностью, чем свободный РХ. [4]
Алюминий весьма склонен к образованию комплексов типа двойных солей. Степень устойчивости таких комплексов в водном растворе сильно зависит от свойств аниона. Так, довольно устойчивы комплексные фториды типа криолита Na3 [ AlF6 ], а также некоторые более сложные формы. [5]
Изменение энтропии AS при образовании комплексов НТА типа 1: 1 на 10 - 20 кал / ( моль - град) меньше такового для комплексов ЭДТА. Это понятно, потому что НТА - четырехдентатный лиганд и ионы металла с координационным числом 6 при комплексообразо-вании теряют не все координированные молекулы воды. Ионы железа ( III) удерживают больше молекул растворителя, чем катионы двухвалентных металлов, и образование комплексов железа ( III) сопровождается большим изменением энтропии образования. [6]
В работе Кузьменко [61] показано образование комплексов типа HLnX ( где Ln - La, Ce, Nd) и ЬщХ3 с ГМДТА. Увеличение центрального цикла комплексов приводит к уменьшению прочности нормальных комплексов и незначительному уменьшению прочности водородных комплексов для щелочноземельных металлов. [7]
Водородные связи могут привести к образованию комплексов типа LM. Различают внутри-и межмолекулярные Н - связи. Относительно природы Н - связей нет единой точки зрения [7, 14], в частности является спорным отнесение их к типу химических связей. [8]
Жесткие стерические требования, обусловливающие возможность образования комплексов типа хозяин-гость, предполагают, что это явление может быть стереоселективным. [9]
Однако в более щелочных растворах возможно также образование комплексов типа I. Иногда, по-видимому, образуются смешанные комплексы. Так, известно, что гидроокись кальция значительно повышает интенсивность окраски ализарината алюминия; это предлагалось использовать для фотометрического определения кальция. [10]
В настоящее время принято считать, что образование комплекса типа МА. [11]
Вышеуказанный факт можно было бы объяснить также образованием комплексов типа Me [ NbOX5 ], которые должны быть стабильнее комплексов типа Me [ NbX. Благодаря этому отношение NbOJs / NbJ5 в газовой фазе уменьшится, что приведет к выделению более чистого ниобия. [12]
Вышеуказанный факт можно было бы объяснить также образованием комплексов типа Me [ NbOX5 ], которые должны быть стабильнее комплексов типа MefNbX. Благодаря этому отношение NbOJ3 / NbJ5 в газовой фазе уменьшится, что приведет к выделению более чистого ниобия. [13]
При высоких значениях рН эта тенденция проявляется в образовании комплекса биуретового типа, в котором Си ( II) координирована только с атомами азота пептидной связи. [14]
В работах В. В. Коршака и Н. Н. Лебедева [17, 18] высказано предположение об образовании комплексов типа. [15]
Страницы: 1 2 3 4