Образование - адсорбированный комплекс
Cтраница 1
Образование адсорбированных комплексов, содержа-ших эти ионы, облегчает стадию передачи электронов от сульфида окислителю и способствует окислению минералов в более мяг-ких окислительных режимах. SO 2Г, S2O 2Г, а также другие соединения, присутствие которых установлено по наличию разности между содержанием общей серы и перечисленных форм. [1]
Представления об образовании адсорбированного комплекса НСОН положены в основу механизма синтеза углеводородов, предложенного Андерсоном [13] и авторами работы [30], исследовавшими синтез Фишера-Тропша на никелевом катализаторе. По мнению Башкирова с сотрудниками [31, 32], и на железном катализаторе следует ожидать образования неустойчивого промежуточного комплекса, состоящего из атомов углерода и водорода, который является родоначальником как углеводородов, так и спиртов. [2]
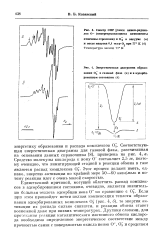 |
Спектр ЭПР [ смеси аннон-радикалов О - ( неперекрывающиеся компоненты.| Энергетическая диаграмма образования O. j в газовой фазе ( а и в адсорбированном состоянии ( б. [3] |
Если при этом произойдет почти полная компенсация теплоты образования адсорбированных комплексов Оз ( рис. 4, б), то энергия активации их распада сильно снизится, и реакция обмена станет возможной даже при низких температурах. [4]
Когда на активном никелевом окисле предварительно адсорбируют СО, а затем впускают кислород, то, как показали Тейхнер и др. [25], имеет место взаимодействие с образованием адсорбированного комплекса, который следует отличать от адсорбированного углекислого газа. Такое заключение вытекает из наблюдений за изменениями окраски и проводимости. Оно по сути совпадает с выводом, сделанным ( см. раздел II, Б) на основании калориметрических данных для прокаленной окиси. [5]
Когда на активном никелевом окисле предварительно адсорбируют СО, а затем впускают кислород, то, как показали Тсйхнср и др. [25], имеет место взаимодействие с образованием адсорбированного комплекса, который следует отличать от адсорбированного углекислого газа. Такое заключение вытекает из наблюдений за изменениями окраски и проводимости. Оно по сути совпадает с выводом, сделанным ( см. раздел II, Б) на основании калориметрических данных для прокаленной окиси. [6]
А - константа для данного класса веществ; у - поверхностное натяжение подвижной фазы; N - число Авогадро; ДЛ - уменьшение общей неполярной поверхности в результате образования адсорбированного комплекса. [7]
А - константа для данного класса веществ; - у - поверхностное натяжение подвижной фазы; N - число Авогадро; ДЛ - уменьшение общей неполярной поверхности в результате образования адсорбированного комплекса. [8]
На основании данных по адсорбции индия из роданидных растворов [106, 107] и по определению порядка реакции по ионам SCN [144, 145] в работе [120] сделан вывод, что замедленной стадией при разряде является образование адсорбированного комплекса In ( SCN) 2, который затем обратимо присоединяет три электрона, и отмечается, что в случае галогенидных растворов интерпретация опытных данных на основе механизма, предложенного для роданид-ионов, затруднительна. В работах [146, 147] предполагается, что восстановление индия идет по двум параллельным путям - на чистой поверхности ртути и на поверхности, покрытой адсорбированными роданид-ионами. Изложенные выше работы, как видно, по своим результатам согласуются с данными по влиянию анионов и комплексообразования на анодный процесс. [9]
По мнению автора, наличие токсических свойств по отношению к платине, видимо, определяется структурой rf - слоя адсорбированного металла. Отравление платины ионами металлов включает, вероятно, образование адсорбированных комплексов, которые в некотором отношении можно рассматривать как интерметаллические соединения. Токсичность, а именно способность образования прочных адсорбционных связей, свойственна, видимо, тем металлам, у которых все пять орбит d - оболочки, непосредственно предшествующих s - и р-валентным орбитам, заняты электронными парами, по крайней мере одиночными rf - электронами. [10]
На полярограммах ( рис. 44) наблюдаются две пары симметричных катодно-анодных пиков, для которых отношение 1 раА рк1 - Оба редокс-процесса соответствуют одноэлек-тродным переходам. Такая форма полярограммы отвечает адсорбции обеих редокс-форм. Лейкометиленовый синий обладает неустойчивой электронной конфигурацией, его высшая молекулярная орбиталь является разрыхляющей. Поэтому это соединение имеет электроно-донорные свойства. Метиленовый синий, напротив, обладает электроноакцепторными свойствами. Для систем такого типа характерно образование комплекса с переносом заряда. Сближение молекул лейкометиленового синего и метиленового синего в адсорбционном слое способствует перекрыванию я-орбиталей, а энергия адсорбции равна энергии образования адсорбированного комплекса. Эффект образования промежуточного активированного комплекса ( сэндвича) обнаруживается только в таких методах, в которых возможна регистрация процесса за период жизни одной капли ртути. [11]
Оба редокс-процесса соответствуют одноэлек-тродным переходам. Такая форма полярограммы отвечает адсорбции обеих редокс-форм. Лейкометиленовый синий обладает неустойчивой электронной конфигурацией, его высшая молекулярная орбиталь является разрыхляющей. Поэтому это соединение имеет электроно-донорные свойства. Метиленовый синий, напротив, обладает электроноакцепторными свойствами. Для систем такого типа характерно образование комплекса с переносом заряда. Сближение молекул лейкометиленового синего и метиленового синего в адсорбционном слое способствует перекрыванию л-орбиталей, а энергия адсорбции равна энергии образования адсорбированного комплекса. Эффект образования промежуточного активированного комплекса ( сэндвича) обнаруживается только в таких методах, в которых возможна регистрация процесса за период жизни одной капли ртути. [12]
Страницы: 1