Образование - внешнесферный комплекс
Cтраница 1
Образование внешнесферных комплексов, по всей вероятности, может во многих случаях сопровождаться небольшими изменениями энтропии и энталь-пии, так как при этом практически отсутствует дегидратация, следовательно, мало меняется число частиц, а сами взаимодействия происходят только через промежуточную гидратационную сферу. [1]
Образование внешнесферных комплексов происходит значительно чаще, чем это обычно принято считать. Нередко в растворе в соизмеримых количествах присутствуют внутри - и внешнесферные комплексы и не всегда есть достаточно надежные экспериментальные методики, чтобы раздельно фиксировать наличие частиц того или иного типа. Это обстоятельство, по-видимому, явилось одной из причин противоречивости данных по константам устойчивости, найденных разными методами, когда один из методов в состоянии фиксировать наличие, например, только внутрисферных комплексов, а другой - сумму тех и других. [2]
Перенос электронов осуществляется в результате образования внешнесферного комплекса. В этом случае перекрывание орбиталей двух реагирующих форм мало. [3]
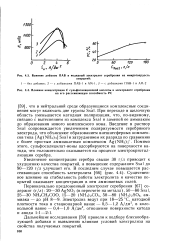
Линхард [142] первый показал, что спектральные изменения, показанные на рис. 1.4, обусловлены образованием внешнесферных комплексов. [4]
Эти цифры лишь немного меньше представленных в табл. 3.12, которые могут быть обусловлены константой равновесия образования внешнесферного комплекса, меньшей чем единица, для комплексов с нейтральными аминами в качестве лигандов. [5]
Во всяком случае, образование ионной пары [ Co ( NH3) 5H2O ] 3 1 SOl - точно установлено и скорость реакции замещения воды на сульфат-ион находится в прямой зависимости от концентрации этого аниона. Образование внешнесферных комплексов обнаружено для большинства комплексных соединений. Но пока еще нельзя утверждать, что они во всех случаях определяют скорость и механизм реакций. [6]
Уменьшение электростатического отталкивания между реагентами, очевидно, связано с ионным потенциалом ионов-активаторов, и следует ожидать, что эффективность их будет тем больше, чем меньше их размер и чем больше заряд. Принято считать, что эти ионы действуют путем образования внешнесферных комплексов с реагентами, что способствует сближению между последними. [7]
 |
Влияние добавок ПАВ в иодидный электролит серебрения на микротвердость.| Влияние концентрации С сульфосалициловой кислоты в электролите серебрения на его рассеивающую способность PC. [8] |
При переходе в щелочную область уменьшается катодная поляризация, что, по-видимому, связано с вытеснением из комплекса Ssai и заменой ее аммиаком до образования нового комплексного иона. Введение в раствор Ssal сопровождается увеличением поляризуемости серебряного электрода, что объясняют образованием внешнесферных комплексов типа [ Ag ( NHs) 2 ] Ssal и затруднением их разряда по сравнению с более простым аммиакатным комплексом Ag ( NH3) 2 - Помимо этого, сульфосалицилат-ионы адсорбируются на поверхности катода, что положительно сказывается на процессе электрокристаллизации серебра. [9]
В настоящее время известно очень мало примеров каталитических реакций, активируемых путем ослабления электростатического отталкивания. Авторы считают, что сближение между реагентами в этой реакции сильно облегчается в результате образования внешнесферного комплекса. [10]
В рассмотренном случае активирование должно быть тем больше, чем легче поляризуется активатор. Предполагают, что в ходе реакции образуется комплекс [ Ре ( рЬеп) з ] 8208Г, в котором сильно поляризующаяся молекула активатора играет существенную роль не только в процессе образования внешнесферного комплекса, но и в акте переноса электрона между катализатором и реагентами. [11]
Страницы: 1