Образование - смешанный комплекс
Cтраница 2
Это может свидетельствовать об образовании смешанных комплексов типа 8с ( Ш3) г ( СЮ4) 3 гл: ТБФ. [16]
При этом в принципе происходит образование смешанных комплексов. Координация молекул растворителя обычно не принимается во внимание. [17]
В щелочных растворах следует допустить образование смешанных комплексов, в состав которых входят и компоненты буферных смесей ( NH3, BOI), и протонированная форма лиганда. Существование таких частиц при высоких рН вполне реально, если учесть рК кислотной диссоциации тиолов. [18]
Однако это не исключает возможности образования смешанных комплексов и другого состава. [20]
В общем случае для определения констант образования смешанных комплексов необходимо знать распределение ионов металла и подвижных лигандов между раствором и фазой сорбента. [21]
Фридман и др. [333-339] изучили процессы образования различных смешанных комплексов. В работе [334] использован потенциометрический метод измерения равновесных концентраций ионов РЬ2 и Cd2 в присутствии различных галогенидов и их смесей и устано. По растворимости оксалатов кадмия, серебра, свинца и иттрия в растворах, содержащих этилендиамин ( en) и К2С2О4, найден состав и вычислены константы устойчивости соответствующих соединений. [22]
В области значений рН 2 - 6 образования смешанного комплекса не происходит; при рН 6 - 8 - происходит частично, но большая часть азосоединення остается в свободном состоянии в хлороформном слое и затемняет спектрфсто етрн ческую картину образования тройного комплекса. При более высоких значениях рН ( 8 - 13) происходит преимущественное образование смешанного комплекса, но наряду с его экстракцией в органическую фазу идет процесс флотации, образуется стойкая пена, механически задерживающая в водной фазе частички смешанного комплекса. [23]
 |
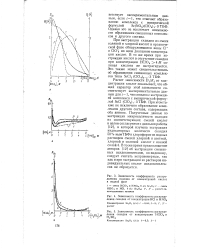
Определение числа молекул винной кислоты, участвующих в образовании гетероцентрового комплекса в системе ионы железа ( III - галлия ( III - винная кислота. [24] |
Как видно из рис. 5.35, в образовании смешанного комплекса принимают участие две молекулы винной кислоты. [25]
При более высоких значениях рН, когда условия образования смешанного комплекса наиболее благоприятны, для него нет исходного материала - купфероната тория, поскольку при рН 9 - 12 он практически не образуется. [26]
 |
Зависимость скорости образования тельно, при достаточно боль-радикалов от начальной концентрации fvi. [27] |
Для подтверждения правильности предлагаемой схемы распада гидроперекиси с учетом образования смешанного комплекса измерены константы равновесия образования комплексов Cu. [28]
В присутствии комплексонов или сульфосалицилатов каталитический процесс связан с образованием смешанных комплексов. [29]
Значительную роль в этой реакции играют процессы комплексообразования, причем возможно образование смешанного комплекса: реагент - железо ( III) - перекись водорода. В результате термодинамической неустойчивости смешанного комплекса происходит окисление реагента по месту двойной связи. [30]
Страницы: 1 2 3 4