Образование - метафосфат
Cтраница 1
Образование метафосфата, очевидно, приводит к получению повышенных результатов. [1]
На образование поликристаллического метафосфата скандия общей формулы ScP309 из кислого фосфата Sc ( H2P04) 3 указано в работе [37], причем в зависимости от режима термообработки образуется его А - или С-форма. [2]
В условиях трения при умеренных температурах образование метафосфатов металлов, по-видимому, маловероятно. Однако в условиях резания, когда температуры достаточно высоки, это вполне возможно. [3]
В соответствии с утверждением, что фосфорилирующие свойства моноэфиров фосфатов в присутствии карбодиимидов обязаны образованию мономерного метафосфата, находится факт, что монобен-зилфосфит ( равноценный диалкилфосфату, не способному образовывать метафосфат) в присутствии ди-л-толилкарбодиимида является очень плохим реагентом для введения фосфитной группы. [4]
Разложение сопровождается выделением паров воды и аммиака и образованием метафосфата натрия NaPO3 в виде перла. [5]
Это справедливо и для ангидридов фосфорных и карбоновых кислот. Во втором случае, вероятно, происходит прямая нуклеофильная атака на атом фосфора, которая протекает более медленно; однако образования мономерного метафосфата как стадии, лимитирующей скорость реакции, полностью исключить нельзя. [6]
Механизм процесса дегидратации кислых ортофосфатов калия был изучен Остерхельдом и Одриетом [8] с помощью термографического, рентгенографического и химических методов анализа. На основании этих исследований установлено, что при любых соотношениях одно - и двузамещенных ортофосфатов калия при 245 С сначала образуется трехзамещенный пирофосфат калия, а при дальнейшем нагревании состав образующихся веществ зависит от соотношения исходных одно - и двузамещенных ортофосфатов. В случае избытка однозамещенного фосфата при 255 С происходит образование метафосфата калия, а при избытке двузамещенного фосфата калия получается триполифосфат калия. [7]
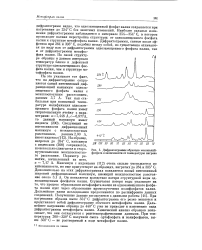 |
Дифрактограммы образцов монокалий-фосфата в зависимости от температуры нагрева. [8] |
Максимум с индексами ( 112) очень сильно уменьшается по интенсивности, но еще присутствует на образцах, нагретых до 284 и 305 С. Дополнительно на этих дифрактограммах появляется новый интенсивный широкий дифракционный максимум, имеющий межплоскостное расстояние около 3 1 А. Он появляется вследствие потери структурной воды од-нозамещенным фосфатом калия. Ступенчатая потеря воды указывает на то, что процесс образования метафосфата калия из однозамещенного фосфата калия идет через образование промежуточных полифосфатов калия. Дальнейшие наши исследования продолжаются по расшифровке данных соединений. При нагревании образца выше 354 С дифрактограмма его резко меняется и представляет собой дифрактограмму обычного метафосфата калия. Дальнейшее нагревание образца до 440 С уже не приводит к изменению вида Дифрактограммы метафосфата калия. Химический анализ образцов показывает, что они согласуются с рентгенографическими данными. При температурах 200 - 350 С получали смесь ортофосфата и полифосфатов, выше 350 С - не растворимый в воде метафосфат калия. [9]
При ферментативном гидролизе моноэфиры тиофосфата реагируют быстрее зфиров фосфата, тогда как при неферментативном гидролизе наблюдается обратная закономерность. С другой стороны, при неферментативном гидролизе триэфиров производные тиофосфата реагируют медленнее. Считают, что триэфиры гидролизуются по ассоциативному механизму, который предусматривает уменьшение кратности связи РО ( или PS) и увеличение заряда атома кислорода ( серы) в переходном состоянии, тогда как гидролиз моноэфиров протекает по механизму элиминирования с образованием метафосфата, при котором кратность связи РО ( или P S) увеличивается, а заряд атома кислорода в переходном состоянии уменьшается ( разд. [10]
Страницы: 1