Образование - мицелла
Cтраница 1
Образование мицелл обусловлено действием дисперсионных сил между цепями углеводородов. Присутствие сильнополярных молекул воды, по-видимому, сильно нарушает этот механизм, так что аномальная функция смешения достигает минимума. [1]
 |
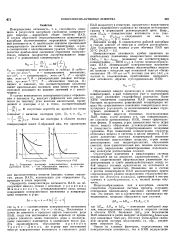
Типичны изотермы поверхностного натяжения. [2] |
Образование мицелл происходит в узком интерпале концентраций, к-рый становится уже и определенней по мере удлинения гидрофобных радикалов. Выше ККМ увеличение содержания ПАВ сопровождается быстрым возрастанием равновесной концентрации мицелл без существенного изменения концентрации молекулярного р-ра вплоть до возникновения новых структурных изменений в системе. [3]
Образование мицелл в растворах коллоидных ПАВ, как и адсорбция молекул ПАВ в поверхностном слое, протекает самопроизвольно. При концентрации ПАВ ниже ККМ энергия Гиббса системы уменьшается за счет адсорбции ПАВ на границе раствор - воздух. При этом углеводородный радикал молекулы ПАВ выталкивается из воды в газовую фазу. Так происходит вплоть до достижения предельной емкости адсорбционного слоя. [4]
 |
Типичные изотермы поверхностного натяжения. [5] |
Образование мицелл происходит в узком интервале концентраций, к-рый становится уже и определенней по мере удлинения гидрофобных радикалов. Выше ККМ увеличение содержания ПАВ сопровождается быстрым возрастанием равновесной концентрации мицелл без существенного изменения концентрации молекулярного р-ра вплоть до возникновения новых структурных изменений в системе. [6]
Образование мицелл характерно для водных растворов моющих веществ ( например, мыл - щелочных солей высших жирных кислот) и некоторых органических красителей с большими молекулами. [7]
 |
Растворы мицеллярных коллоидов. молекулярный раствор ( а, коллоидные растворы со сферическими ( Г и пластинчатыми ( в мицеллами. [8] |
Образование мицелл характерно для водных растворов моющих веществ ( например, мыл - щелочных солей высших жирных кислот) и некоторых органических красителей с большими молекулами. В других средах, например в этиловом спирте, эти вещества растворяются с образованием молекулярных растворов. [9]
 |
Схема изменения Мицеллярная масса достигает20000. физико-химических и тех - В разбавленных молекулярных. [10] |
Образование мицелл в мыльных растворах - самопроизвольный, термодинамически выгодный процесс. Дело в том, что молекулы мыл обладают очень резко выраженной ди-фильностью, так как имеют в своем составе, с одной стороны, весьма гидрофильную полярную группу ( - COONa), с другой-очень длинную неполярную углеводородную цепь. Молекулы мыла, образуя мицеллы, ориентируются углеводородными цепями друг к другу; создается углеводородное ядро, а полярные группы составляют наружную обкладку мицелл. При этом молекулы мыла частично диссоциируют, так что вокруг ядра образуется двойной электрический слой ионов, который хорошо гидратируется. Этим объясняется высокая растворимость щелочных мыл в воде: чтобы мицеллы, поверхность которых хорошо гидратируется, внедрились в объем водной фазы, не надо затрачивать работу на раздвигание молекул воды. [11]
Образование мицелл в водных растворах ПАВ при достижении критической концентрации, характерной для каждого вещества и зависящей от его строения, следует рассматривать как возникновение двухфазных систем высокой степени дисперсности. В этих системах длинноцепочечные поверхностно-активные ионы ( или молекулы) находятся в равновесии с мицеллами различной структуры. Присутствие в растворах ПАВ электролитов смещает это равновесие и приводит к уменьшению критической концентрации мицеллообразования. [12]
Образование мицелл не представляет собой образования ноьий макроскопической фазы и, следовательно, не характеризуется един - - - етвенной критической точкой перехода. Использование термина критическая концентрация мицеллообразования может, следовательно, ввести в заблуждение, и в некоторых случаях мы будем избегать употребления этого термина. [13]
Образование мицелл характерно для водных растворов моющих веществ ( например, мыл - щелочных солей высших жирных кислот) и некоторых органических красителей с большими молекулами. В других средах, например в этиловом спирте, эти вещества растворяются с образованием молекулярных растворов. [14]
 |
Схема мицеллы в неполярной среде. [15] |
Страницы: 1 2 3 4