Образование - молекула - метан
Cтраница 1
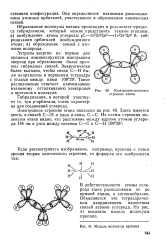 |
Модель молекулы пропана. [1] |
Образование молекулы метана происходит в результате процесса гибридизации, который можно представить такими этапами: а) возбуждение атома углерода: 6С - Is22s22p2 - Is22s ] 2p3 б; гибридизация орбиталей возбужденного атома; в) образование связей с атомами водорода. [2]
При образовании молекулы метана СН4 р3 - гибрид-ные орбитали атома углерода перекрываются с s - орби-талями атомов водорода, что представлено на рис. 19.2. Гибридные орбитали атома углерода направлены к вершинам воображаемого тетраэдра, что объясняет тетра-эдрическую форму молекулы метана. [3]
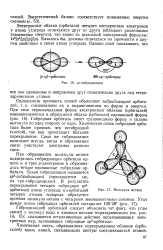 |
Молекула метана. [4] |
При образовании молекулы метана подверглись гибридизации орбитали одного s - и трех р-электронов и образовались четыре одинаковые гибридные орбитали. [5]
В действительности процесс образования молекулы метана не проходит через стадию валентного состояния изолированного атома. При сближении атомов уже начинается их связывание друг с другом в молекулу, хотя сначала и в очень рыхлую, и изменение характера орбиталей сопутствует этому процессу, происходя постепенно. [6]
Например, при образовании молекулы метана гибридизации подвергаются орбитали атома углерода: одна s - и три р-орбитали. Вид и число орбиталей, участвующих в гибридизации, определяет ее тип. Так, в метане проявляется р3 - гибридизация. В пространстве эти орбитали расположены относительно друг друга под одинаковыми углами и направлены к вершинам тетраэдра. [7]
Однако одностадийного распада каждой молекулы ацетальдегида с образованием молекул метана и моноксида углерода не происходит. Кинетические результаты подсказывают механизм, который предполагает, что вначале молекула ацетальдегида распадается на метальный и формильный радикалы. Продукты образуются в последующих реакциях между этими радикалами, ацетильным радикалом и самим ацетальдегидом. [8]
 |
Взаимное расположение гибридных sp - облаков.| Взаимное расположение гибридных 5р3 - об-лаков. [9] |
Такая гибридизация осуществляется, например, в возбужденном атоме углерода при образовании молекулы метана СЩ. [10]
Из этих данных ясно, почему использование гибридных орбиталей, например хр3 - орбиталей в связывании одного атома углерода с четырьмя атомами водорода при образовании молекулы метана, приводит к возникновению более прочных связей. [11]
Из этих данных ясно, почему использование гибридных ор-биталей, например 5р3 - гибридных орбиталей в связывании одного атома углерода с четырьмя атомами водорода при образовании молекулы метана, приводит к возникновению более прочных связей. [12]
Из этих данных ясно, почему использование гибридных ор-бпталей, например 5 / э3 - гибридных орбиталей в связывании одного атома углерода с четырьмя атомами водорода при образовании молекулы метана, приводит к возникновению более прочных связей. [13]
 |
Изображение гибридной орбитали.| Типы гибридизации, геометрические формы частиц и углы между связями. [14] |
Следует различать стадию возбуждения атома, например, углерода ( переход ls22s22p2 - Is22sl2p3), что имеет место в действительности для свободного атома при затрате энергии, и стадию гибридизации, как наглядный способ изображения результата связывания, например, атома С с четырьмя атомами Н при образовании молекулы метана. Гибридизация валентных орбиталей атома, образующего связи с более чем одним атомом-партнером, сама по себе не есть следствие его возбуждения; она постулируется только для интерпретации эквивалентности сформированных связей. [15]
Страницы: 1 2