Образование - молекула - водород
Cтраница 1
Образование молекулы водорода происходит следующим образом. При сближении двух атомов водорода их электроны образуют общую пару, которая совершает движение в поле обоих ядер. В результате каждый из атомов, составляющих молекулу Н2, имеет устойчивую оболочку из двух электронов. [1]
Образование молекулы водорода объясняется с помощью метода молекулярных орбиталей следующим образом. При сближении двух атомов водорода происходит перекрывание их электронных орбиталей, причем из двух одинаковых ls - орбиталей образуются две молекулярные орбитали, одна из которых - от сложения атомных орбиталей, другая - от вычитания атомных орбиталей. [2]
Поскольку образование молекулы водорода возможно только при антипараллельных спинах электронов, полный спин молекулы водорода должен быть равным нулю. Отсюда следует, что и магнитный момент молекулы водорода должен быть равен нулю. Поэтому водород должен быть диамаг-нетиком. Это заключение подтверждается экспериментом. [3]
Рассмотрим образование молекулы водорода из двух атомов водорода. [4]
При образовании молекулы водорода электронный дублет как бы обслуживает оба ядра, в результате чего они оказываются прочно связанными в единую молекулу. Аналогичное наблюдается и в молекулах других веществ. [5]
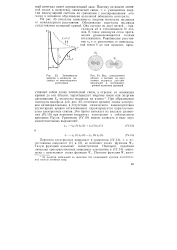 |
Вид электронного облака в системе из двух атомов водорода для симметричной и антисимметричной волновых функций. [6] |
При образовании молекулы водорода ( см. рис. 33, сплошная кривая) спины электронов антипараллельны, а отсутствие химического взаимодействия ( пунктирная кривая отталкивания) характеризуется параллельностью электронных спинов. Это прямо вытекает из анализа уравнения (IV.10) при перемене координат электронов с соблюдением принципа Паули. [7]
При образовании молекулы водорода электронный дублет как бы обслуживает оба ядра, в результате чего они оказываются прочно связанными в единую молекулу. Аналогичное наблюдается и в молекулах других веществ. [8]
Медленность стадии образования молекул водорода из атомов приводит к повышению концентрации адсорбированного атомарного водорода на поверхности металла, которая легко может быть обнаружена по замедлению спада потенциала после размыкания поляризующего тока, как это наблюдалось, например, П. Д. Луковцевым и С. Д. Левиной [ 35J для случая никеля в щелочных растворах. Существенные данные о медленности стадий, следующих за стадией разряда, получаются также при наблюдении проникновения водорода внутрь металла. Задержки в удалении адсорбированного водорода, приводящие к повышению его концентрации на поверхности, приводят также к усилению его диффузии в металл. [9]
Представления об образовании молекулы водорода, развитые Гейтлером и Лондоном, были распространены и на более сложные молекулы. На этой основе возникла теория образования химических связей, которая получила название метода валентных связей. Этот метод основан на представлении о том, что атомы в молекуле удерживаются посредством одной или нескольких электронных пар, причем эти связи тем прочнее, чем в большей степени перекрываются электронные облака взаимодействующих атомов. Обычно большая степень перекрывания электронных облаков наблюдается на прямой, соединяющей центры атомов. Комбинации двухэлектронных двухцентровых сгзязей, которые отражают электронную структуру молекулы, называют валентными схемами. [10]
Следующая стадия - образование молекул водорода из атомов-протекает с некоторой ограниченной скоростью. [11]
Какие силы вызывают образование молекулы водорода и обеспечивают ее устойчивость. При сближении двух атомов водорода, имеющих одиночные электроны с противоположными спинами, образуется молекула с общей парой электронов. В пространстве между ядрами обоих атомов возникает область повышенной плотности отрицательного электрического заряда. Это вызывает стягивание ядер атомов водорода друг к другу, вследствие чего частично перекрываются их электронные облака. В пространство, занимаемое облаком одного электрона, проникает облако другого электрона. [12]
Рассмотрим, например, образование молекулы водорода Н2, где рассуждения об электрическом притяжении, казалось бы, явно неприменимы. Образование устойчивой электронной конфигурации в данном случае происходит путем обобществления электронов. Такое объяснение образования химической связи за счет взаимодействия электронов впервые было предложено американским физико-химиком Дж. Согласно Льюису, каждый, из двух атомов, вступающих в химическую связь, предоставляет в общее владение по одному электрону так, что пара электронов принадлежит одновременно двум атомам. При этом атомы стремятся достроить свои электронные оболочки до конфигурации инертного газа. [13]
 |
Взаимодействие двух атомов водорода. Притяжение электронов ядрами, отталкивание электронов и отталкивание ядер.| Распределение отрицательных зарядов в атомах и молекуле водорода. [14] |
Ковалентная связь, определяющая образование молекулы водорода, обеспечивается силами электростатического притяжения между отрицательно заряженным облаком, соответствующим новому распределению электронов, и положительными зарядами ядер. [15]
Страницы: 1 2 3 4