Образование - нитрит
Cтраница 3
При облучении водных растворов щелочей в атмосфере воздуха наблюдается радиационно-химический процесс связывания атмосферного азота с образованием нитрита и нитрата. Выход этого процесса равен около 0 1 молекулы / 100 эв и не зависит от концентрации щелочи, в пределах рН от 9 0 до 14 0 и давления воздуха до 25 атм. [31]
Свежее коровье молоко ускоряет восстановление нитрата ацеталь-дегидом в такой степени, что при подходящих условиях опыта образование нитритов можно обнаружить уже через 1 - 2 минуты. [32]
Свежее коровье молоко ускоряет восстановление нитратов альдегидами в такой мере, что при соответствующих условиях опыта образование нитрита можно обнаружить уже по истечении 1 - 2 минут. Кипяченое молоко в присутствии альдегида, а также свежее молоко без альдегида не оказывают сами по себе никакого влияния на восстановление нитратов. [33]
Действительно, при биологической нитрификации происходит переход от аммонийных форм N / NH3 в нитратные с образованием промежуточных нитритов N / NOg, которые, находясь в воде, отчасти токсичны для детей, и эти недостатки можно предотвратить при осуществлении процесса нитрификации. С другой стороны, в водном источнике возможны обратные процессы, известные как ассимилятивное восстановление. В конечном счете при нитрификации потребляется кислород, а следовательно, и энергия, тогда как при диссимилятивном восстановлении, когда нитраты превращаются в газообразный азот, высвобождаемая часть кислорода, использованного ранее для нитрификации, потребляется на окисление загрязнений, содержащих соединения углерода. Общая тенденция поэтому заключается в полном удалении азота. Возможны два способа: физико-химическое удаление; биологическая нитрификация / денитрификация. [34]
Избегают использования избытка НС1 для того, чтобы ограничить образование хлорида Кроме того, вследствие слабой диссоциации HNOj образование нитрита будет происходить лишь в небольшой степени. [35]
В следует учитывать, что на переход 1 мг аммонийного азота в нитраты требуется 4 57 мг кислорода, а для образования нитритов - 3 43 мг. [36]
По условиям техники безопасности при пуске контактных аппаратов н во время нормальной эксплуатации на тарелках газовых холодильников-промы-вателей поддерживают кислую среду для предотвращения образования нитрита аммония. [37]
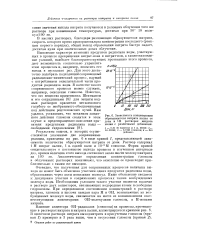 |
Зависимость концентрации образующегося нитрита калия от дозы в 1М растворах нитрата калия с различными добавками.... -. - - 1 - 0 01 М глюкоза и 1 н. КОН. 2. [38] |
В кислых растворах, благодаря разложению образующегося нитрита, скорость которого прямо пропорциональна концентрации последнего ( реакция первого порядка), общий выход образования нитрита быстро падает, достигая нуля при значительных дозах облучения. [39]
Количество кислорода, заключающегося в нитратах н нитритах, может быть определено из приведенных выше уравнений, из которых видно, что на две части азота для образования нитритов требуется шесть частей кислорода, а для образования нитратов - еще две части кислорода, а всего 8 частей. Атомный вес азота N 14, а кислорода О 16, тогда на окисление 14 - 2 28 частей азота требуется 8x16 128 частей кислорода или на 1 мг азота 128: 28 - 4 57 мг кислорода. [40]
 |
Зависимость концентрации образующегося нитрита калия от дозы в 1 н растворе КОН в атмосфере воздуха. [41] |
Увеличение давления воздуха над раствором до 25 атм ( такие опыты велись в специально сконструированных в лаборатории ампулах из нержавеющей стали, снабженных манометром) не сказывалось на скорости процесса и выходе образования нитрита. [42]
Для описываемого здесь способа нитрования очень важно то обстоятельство, что тетранитрометан в присутствии концентрированных щелочей разлагается с образованием нитроформа и что с повышением концентрации щелочи образование нитроформа-выступает на первый план за счет образования нитрита. В присутствии слабых щелочей тетранитрометан также может полиостью распадаться на нитроформ и азотную кислоту, если реакцию вести в спиртовом или ацетоновом растворе. [43]
Другим преимуществом этой конструкции является то обстоятельство, что образующиеся в процессе окисления газы, препятствующие работе биофильтров, удаляются из толщи загрузки, благодаря чему в нижних слоях загрузки продолжается окислительный процесс с образованием нитритов и нитратов, чем и достигается нужная степень очистки. [44]
Кристаллогидраты отличаются различными температурами плавления: четырех-водная соль плавится при 42 7 С, трехводная при 51 1 С, безводная при 561 С, но уже при 500 С она начинает разлагаться с образованием нитрита кальция, который при дальнейшем нагревании распадается на СаО и МСЬ. Насыщенный раствор, содержащий 78 9 % Ca ( NO3h, кипит под атмосферным давлением при 151 С. [45]
Страницы: 1 2 3 4