Образование - бикарбонат
Cтраница 2
В присутствии карбонатов щелочных металлов нужно принять во внимание образование бикарбонатов по ниже изложенной схеме. При щелочных землях, карбонаты которых в воде почти нерастворимы, дело обстоит иначе. W i п k 1 е г у ( подтверждено К u s t е г о м и Lung e, см, ниже), при осторожном прибавлении соляной кислоты достигнуть точки, когда вся едкая известь или едкий барит будут нейтрализованы; малые количества СО2, освобождаемые следующей каплей кислоты из углекислых солей, обесцветят фенолфталеин, что укажет на конец реакции. [16]
Понижению температуры плавления системы карбамид - кар-бамат аммония способствует также образование бикарбоната и карбоната аммония. [17]
Помимо состава исходного аммонизированного рассола и его температуры на реакцию образования бикарбоната натрия влияет содержание СОг в жидкости колонн. [18]
Помимо состава исходного аммонизированного рассола и его температуры на реакцию образования бикарбоната натрия влияет содержание СОо в жидкости колонн. [19]
 |
Узел нижней трубной доски колонны синтеза. [20] |
Образовавшийся СО2 в дальнейшем реагирует с аммиаком и водой с образованием бикарбоната и карбоната аммония. [21]
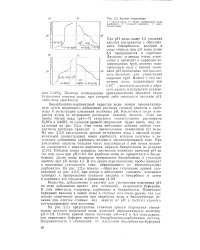 |
Кривые титрования. [22] |
При рН воды выше 4 5 угольная кислота распадается с образованием бикарбоната, который в свою очередь при рН воды выше 8 3 превращается в карбонат. Двуокись углерода очень агрессивна и приводит к коррозии водопроводных труб, поэтому водопроводную воду с низким значением рН необходимо нейтрализовать щелочью для уменьшения коррозии труб. Поэтому наибольшими преимуществами обладает такая технология очистки воды, при которой либо снижается значение рН, либо вода умягчается. [23]
Из уравнения видно, что сода оттитровывается лишь наполовину с образованием бикарбоната, поэтому общая масса СО23 - равна удвоенному объему кислоты, израсходованной на титрование. Втем-ноокрашенных фильтратах СОз определяют разбавлением пробы и после в этой же пробе определяют общую щелочность. [24]
Водные растворы карбонатов натрия и калия поглощают двуокись углерода с образованием бикарбонатов. [25]
На станции карбонизации происходят взаимодействие аммонизированного рассола с углекислым газом, образование бикарбоната натрия и выпадение его в осадок. [26]
Сернистый ангидрид при этом методе взаимодействует с содой, проходя стадии образования бикарбоната и сульфита натрия. Очистка происходит в абсорберах, орошаемых раствором карбоната натрия концентрацией 200 - 280 мг / л, содержащего 50 - 100 г / л сульфата натрия. Образующийся в абсорберах раствор сульфит-бисульфита натрия с некоторым содержанием сульфата натрия разлагают при нормальном или повышенном давлении серной кислотой с концентрацией 78 - 96 % при температуре 35 - 55 С. Получаемый при этом влажный SO2 охлаждают для удаления влаги, сушат и используют в последующем для различных целей. [27]
При наличии в газе углекислоты происходит также и ее связывание с образованием бикарбоната. [28]
При наличии в газе углекислоты происходит также и ее связывание с образованием бикарбоната диэтаноламина. Таким образом, селективность извлечения H2S не достигается. [29]
Увеличение влажности карбоната аммония сдвигает равновесие реакции гидролиза вправо, в сторону образования бикарбоната и карбамата аммония. Насыщение водных растворов карбоната аммония сдвигает равновесие в обратную сторону. [30]
Страницы: 1 2 3 4