Образование - озон
Cтраница 3
Объясните, почему образования озона в газовой фазе по реакции ЗО -, - 2О3 не происходит. [31]
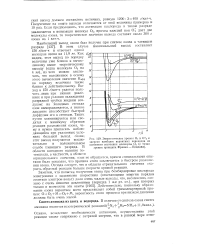 |
Энергетические уровни СЬ и О 2 и. [32] |
Действительно, поскольку образование озона вероятнее всего представляет собой тримолекулярный процесс О О2 М О3 М, вероятность этого процесса при низком давлении должна быть очень малой. [33]
Для истолкования механизма образования озона представляют интерес данные по бомбардировке кислорода медленными электронами. Образование озона они объясняют возникновением возбужденных ионов кислорода. [34]
Пользуясь значениями энтальпии образования озона и атомарного кислорода, приведенными в табл. 7.1, рассчитайте максимальную длину волны фотона, обладающего достаточной энергией для того, чтобы вызвать диссоциацию молекулы озона на молекулу кислорода и атом кислорода, если такой фотон поглощен озоном. [35]
Данные о кинетике образования озона в газовой фазе указывают на то, что при малых концентрациях, по-видимому, удовлетворяются уравнения первого порядка как для образования, так и для распада озона. Если принять для обеих реакций первый порядок и экстраполировать к моменту времени, равному нулю, то увидим, что константа скорости распада более чем на порядок превышает константу скорости образования озона. [36]
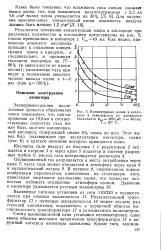 |
Концентрация озона в кислороде в зависимости от влажности последнего v03 400 см3, т 48 сек, t 20 С. [37] |
Экспериментальное исследование процесса образования озона показывает, что при напряжении до 12 5 Кб и соответствующих скоростях газа может быть получен озонированный кислород, содержащий свыше 6 % озона по весу. Этот вывод был подтвержден при эксплуатации озонатора, схема ( рис. 6) и краткое описание которого приводятся ниже. [38]
Ионизация воздуха сопровождается образованием озона и окислов азота, которые вызывают химическое разрушение изоляции кабеля. [39]
Ионизация воздуха сопровождается образованием озона и окислов азота, что вызывает химическое разрушение органической изоляции, содержащей газовые включения. [40]
Ведущую роль в образовании озона обычно отводят окислам азота. Известно, что в естественных условиях азот весьма инертен и не вступает в реакции с кислородом. Этим обеспечивается постоянное соотношение между этими газами в атмосфере. Положение изменяется при высоких температурах. В результате сжигания твердого, жидкого и газового топлива образуется значительное количество окислов азота, особенно много их содержится в выбросах автомашин. При этом образуется атомарный кислород, который может вступать во взаимодействие с углеводородами н другими органическими веществами, содержащимися в выхлопных газах автомашин. В результате образуются как свободные радикалы R, весьма активно вступающие в реакцию и существующие в атмосфере непродолжительное время, так и другие, реакцпонноспособные органические соединения. [41]
Примером фотополимеризации может служить образование озона в процессе облучения кислорода излучением с А 0 2537 мк. [42]
Этим объясняется, почему образование озона из кислорода идет с поглощением значительного количества теплоты. В атоме кислорода электрон с третьего энергетического уровня стремится перейти на второй. [43]
Учитывая это, схема образования озона при электронном ударе может быть представлена следующим образом. [44]
По Маршаллу [33] реакция образования озона при электронном ударе имеет первый порядок по кислороду. [45]
Страницы: 1 2 3 4