Образование - высший оксид
Cтраница 2
Содержание воды переменное, колеблется от 3 5 до 5 молекул воды на формульную единицу. Реагирует с кислотами с частичным растворением и образованием высших оксидов висмута. На холоду в сернокислотном растворе окисляет ионы Мп ( П) до пермаига-иата. [16]
Важнейшей характеристикой топлива является теплота сгорания. Теплотой сгорания вещества называют тепловой эффект реакции окисления кислородом элементов, входящих в состав этого вещества до образования высших оксидов. [17]
Важнейшей характеристикой топлива является теплота сгорания. Теплотой сгорания вещества называют тепловой эффект реакции окисления кислородом элементов, входящих в состав этого вещества до образования высших оксидов. Теплоту сгорания обычно относят к стандартному состоянию ( давление 101 кПа), одному молю топлива и температуре 298 15 К и назначают стандартной теплотой сгорания. [18]
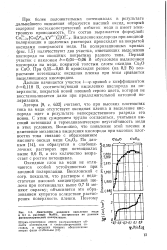 |
Диаграмма анодного окисления меди в 0 1 н. растворе NaOH, построенная по данным фотоэлектрической поляризации. Vf. [19] |
С этим суждением трудно согласиться, учитывая высокий потенциал и термодинамическую неустойчивость меди в этих условиях. Возможно, что появление этой пленки и изменение механизма выделения кислорода при высоких плотностях тока связано с образованием высшего оксида меди Си2Оз - По дан-ным [14], он образуется в слабоще-лочных растворах при потенциалах § выше 0 6 В, а его количество возра - g стает с ростом потенциала. [20]
У молибдена и вольфрама коррозионная устойчивость в кислых средах резко возрастает, поскольку состав их пассивирующих пленок близок к кислотообразующим оксидам соответствующих кислот ( МоО3 и WO3) вследствие повышения стабильности высшей степени окисления в ряду Сг - Mo - W. По этой причине молибден и вольфрам в щелочных средах менее устойчивы, чем хром, для которого не характерно образование высшего оксида на поверхности. [21]
При росте потенциала в пленке появляется примесь Cr ( VI), что приводит к улучшению ее защитных свойств. Степень гидратации пленки уменьшается. Дальнейшее повышение потенциала приводит к образованию высших оксидов хрома. Эти оксиды анодно или химически образуют хроматы, переходящие в раствор. [22]
При росте потенциала в пленке появляется примесь Cr ( VI), что приводит к улучшению ее защитных свойств. Степень гидратации пленки уменьшается. Дальнейшее повышение потенциала приводит к образованию высших оксидов хрома. Эти оксиды анодно или химически образуют хроматы, переходящие в раствор. [23]
Важнейшими характеристиками топлива являются теплота сгорания и теплотворная способность. Теплотой сгорания вещества называют тепловой эффект реакции окисления кислородом входящих в состав этого вещества элементов до образования высших оксидов. Теплоту сгорания обычно относят к стандартным условиям: 298 15 К, давлению 101 кПа, одному молю топлива и называют стандартной теплотой сгорания. [24]
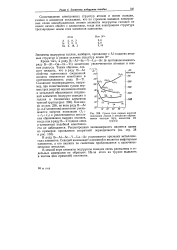 |
Сумма трех первых энергий ионизации атомов и энтальпии образования оксидов Э2О3 элементов III группы. [25] |
Кроме того, в ряду В-Al - Sc-Y-La - Ас ( в противоположность ряду В-Al - Ga-In-Tl) монотонно увеличиваются атомные и ионные радиусы. Таким образом, следует ожидать, что в ряду В-Ас свойства однотипных соединений должны изменяться монотонно в противоположность ряду В-Tl. Как видно из рис. 238, во всем ряду В-Ас ( р - и d - элементов) монотонно уменьшаются энергии ионизации ( / х 2 / з) и увеличиваются энтальпии образования высших оксидов, тогда как в ряду В-Tl ( одних лишь р-элементов) подобной монотонности не наблюдается. Рассмотренная закономерность является одним из примеров проявления вторичной периодичности ( см. стр. [26]
Для многих соединений не удается осуществить реакцию их образования из простых веществ и тем более измерить теплоту образования. Поэтому термохимические расчеты весьма часто производят с использованием теплот сгорания исходных веществ и продуктов реакции. Теплотой сгорания называется тепловой эффект реакции полного сгорания 1 моль данного соединения до образования высших оксидов. [27]
Страницы: 1 2