Образование - перборат
Cтраница 2
Совместное рассмотрение рис. 3 и 4 приводит к следующим выводам. При низких концентрациях В2О3 в электролите - ( 1 - 1 5 г / л) скорость образования пербората натрия очень мала. [16]
Способ получения nej рата, рекомендованный в герм. Он отя чается от способа Арндта1053 присутствием пербората в; 1: осадка в электролите. Если бы образование пербората про дило в результате окисления первичными окислами платины, око наступало бы и при электролизе чистых растворов борат а1 не только в присутствии растворимых карбонатов. [17]
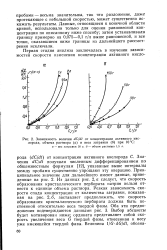 |
Зависимость величин dC / dt от концентрации активного кислорода, объема раствора ( а и веса затравки ( б при 10 С. [18] |
Значения dC / dt получали численным дифференцированием по общеизвестным формулам [12], указанные выше интервалы между пробами существенно упрощают эту операцию. Из данных рис. 2, а следует, что скорость образования кристаллического пербората натрия нельзя отнести к единице объема раствора. Резкая зависимость скорости спада концентрации от количества затравки, показанная на рис. 2, б, заставляет предположить, что скорость образования кристаллического пербората должна быть постоянной относительно веса твердой фазы. Выбор абсциссы будет мотивирован ниже; ордината представляет собой скорость увеличения веса G твердой фазы, отнесенная к весу уже имеющейся твердой фазы. [19]
Страницы: 1 2